йҡҸзқҖе…ЁзҗғиҖҒйҫ„еҢ–з”ҹйҪҝзҡ„еўһж·»д»ҘеҸҠж„ҸеӨ–дәӢж•…еҜјиҮҙйӘЁжҚҹеӨұзҡ„жЎҲдҫӢи¶ҠжқҘи¶ҠеӨҡ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ЁзҗғйӘЁдҝ®еӨҚеёӮеңәйңҖжұӮжӯЈеӨ§е№…еўһж·»[1]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдёәдәҶж”№е–„жӮЈиҖ…з”ҹж¶ҜиҙЁйҮҸ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӨ–科жүӢжңҜдёӯеёёжҺҘзәідәәе·ҘжӨҚе…Ҙзү©�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҘжӣҝжҚўжӮЈиҖ…еӨұж•ҲйғЁдҪҚ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдёҙеәҠдёҠеёёз”Ёзҡ„йҮ‘еұһжӨҚе…ҘиҙЁж–ҷдёҖж ·е№іеёёеҢ…жӢ¬й’ӣеҗҲйҮ‘гҖҒдёҚй”Ҳй’ўд»ҘеҸҠй’ҙ铬еҗҲйҮ‘зӯү�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё»иҰҒдҪңдёәдәәе·ҘжһўзәҪгҖҒйӘЁеҸ–д»Јзү©зӯү�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӣҝжҚўжӮЈиҖ…еҸ—жҚҹжҲ–з—…еҸҳзҡ„зЎ¬иҙЁз»„з»Ү�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ

дёҚй”Ҳй’ўжҳҜз”ҹй•ҝиҫғж—©�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҙЁж–ҷжң¬й’ұиҫғдҪҺзҡ„йҮ‘еұһеҢ»з”ЁжӨҚе…ҘиҙЁж–ҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӣҫеҚ жңүдәҶиҫғеӨ§йғЁеҲҶзҡ„еҢ»з”ЁйҮ‘еұһжӨҚе…Ҙзү©еёӮеңә�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҶз”ұдәҺдёҚй”Ҳй’ўзҡ„еҜҶеәҰиҫғеӨ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӮЈиҖ…ејӮзү©ж„ҹејә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё” Fe зҡ„иҖҗиҡҖжҖ§иҫғе·®�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝз”ЁеҺҶзЁӢдёӯзЈЁжҚҹйҮҠж”ҫзҡ„ NiгҖҒCr зҰ»еӯҗеҜ№з»ҶиғһжҜ’еүҜдҪңз”ЁеӨ§зӯүеӣ зҙ �пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еңЁжӨҚе…ҘдҪ“еёӮеңәдёҠзҡ„еә”用规模еңЁдёҖзӣҙзј©е°Ҹ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҡҸзқҖз”ҹзү©еҢ»з”ЁеҗҲйҮ‘зҡ„жӣҙж–°з”ҹй•ҝ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…·жңүжӣҙеҘҪз”ҹзү©зӣёе®№жҖ§зҡ„й’ӣеҸҠй’ӣеҗҲйҮ‘дә§е“Ғиҝ‘е№ҙжқҘиў«жҷ®йҒҚзҡ„еә”з”ЁдәҺйӘЁз»„з»Үдҝ®еӨҚдёҠ[2]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
зҺ°еңЁ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз»қеӨ§еӨ§йғҪеҢ»з”ЁйҮ‘еұһйӘЁжӨҚе…ҘеёӮеңәзҡ„дә§е“Ғд»ҚжҺҘзәіжЁЎе…·й“ёйҖ зҡ„з”ҹдә§еҠ е·Ҙж–№жі•�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮжӯӨзұ»иҰҒйўҶеҜ№дә§е“Ғе°әеҜёеҢәеҲҶеәҰиҫғе°Ҹ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢж— жі•зҹҘи¶іе·®еҲ«дәәз§ҚгҖҒжҖ§еҲ«гҖҒе№ҙеІҒеҸҠдёӘдҪ“з—…дҫӢзҡ„дёӘжҖ§еҢ–йңҖжұӮ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҗҢж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҮ‘еұһиҙЁж–ҷзҡ„еј№жҖ§жЁЎйҮҸжҜ”йӘЁеӨ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶дёҺйӘЁеӣўз»“дҪҝз”ЁеҸҜиғҪдјҡзҲҶеҸ‘вҖңеә”еҠӣеұҸйҡңвҖқеҫҒиұЎ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҒ’д№…дҪҝз”ЁеҲҷдјҡеҜјиҮҙз—…жӮЈеӨ„жіӣиө·йӘЁиҙЁжқҫж•Ј�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ҡиҮіеј•иө·жӨҚе…ҘдҪ“ж»‘иҗҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙиҺіжӨҚеӨұиҙҘ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝ‘е№ҙжқҘ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶иҖ…们иҜ•еӣҫдҪҝз”ЁеӨҡеӯ”иҙЁж–ҷйҷҚдҪҺжӨҚе…ҘдҪ“еј№жҖ§жЁЎйҮҸ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҸҗй«ҳжӨҚе…ҘдҪ“д№җжҲҗзҺҮ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҸӨжқҝзҡ„еӨҡеӯ”иҙЁж–ҷеҲ¶еӨҮиҰҒйўҶеҢ…жӢ¬зІүжң«еҶ¶йҮ‘жі•[3,4]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжөҶж–ҷжі•[5,6]е’ҢзәӨз»ҙзғ§з»“жі•[7-9]зӯү�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶеқҮеӣ е…¶жүӢиүәзү№зӮ№�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҲ–еӨҡжҲ–е°‘зҡ„еҪұе“ҚиҙЁж–ҷеҠӣеӯҰжҖ§иғҪжҲ–з”ҹзү©еӯҰжҖ§иғҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝе…¶ж— жі•зҹҘи¶іжӨҚе…ҘдҪ“зҡ„еҗ„йЎ№йңҖжұӮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙеӨҡеӯ”з”ҹзү©жӨҚе…ҘдҪ“з”ҹй•ҝиҫғдёәзј“ж…ў�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
йҡҸзқҖ 3D жү“еҚ°иЈ…еӨҮжүӢиүәзҡ„дёҖзӣҙз”ҹй•ҝ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝз”Ё 3D жү“еҚ°жүӢиүәеҲ¶йҖ еҢ»з”ЁеӨҡеӯ”иҙЁж–ҷзҡ„дјҳеҠҝи¶ҠеҸ‘жҳҺжҳҫ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ3D жү“еҚ°жүӢиүәжӢҘжңүжһҒй«ҳзҡ„еҠ е·ҘиҮӘз”ұеәҰ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ідәҺйӘЁз§‘иҙЁж–ҷзҡ„ 3D жү“еҚ°�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еҸҜд»ҘдҪҝз”Ё CTгҖҒMRI зӯүеҢ»еӯҰеҪұеғҸ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡиҝҮзӣҳз®—жңәйҮҚдҝ®жӮЈиҖ…еӨұж•ҲйӘЁжЁЎеӯҗ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҲ¶йҖ еҮәз”ҹзү©еӯҰжҖ§иғҪдёҺеҠӣеӯҰжҖ§иғҪжӣҙдёҺйӘЁеҢ№й…Қзҡ„жӨҚе…Ҙзү©дә§е“Ғ[10,11]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӣҙеҸҜд»Ҙй’ҲеҜ№жҜҸдҪҚжӮЈиҖ…еҲ¶и®ўеҘҮејӮзҡ„жІ»з–—и®ЎеҲ’�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе®һзҺ°дёәйӘЁжӨҚе…ҘжӮЈиҖ…вҖңйҮҸж–ҮдҪ“иЎЈвҖқзҡ„дә§е“Ғе®ҡеҲ¶�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ3D жү“еҚ°з”ұдәҺе…¶еұӮеұӮеҠ е·Ҙзҡ„зү№зӮ№�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜд»ҘеҲ©дҫҝзҡ„еҲ¶йҖ еҮәз§Қз§Қеӯ”еһӢе°әеҜёеҸҠе…·жңүд»ҝз”ҹеӯҰж•Ҳеә”е’Ңз”ҹзү©зӣёе®№жҖ§зҡ„еӨҡеӯ”иҙЁж–ҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҸҗй«ҳжӨҚе…Ҙзү©зҡ„йӘЁеӣўз»“иғҪеҠӣ[10]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D
жү“еҚ°еңЁеҢ»з”ЁйўҶеҹҹдҝқеӯҳйҮҚеӨ§зҡ„еә”з”ЁжҪңеҠӣ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮжң¬ж–Үе°Ҷдё»иҰҒе…Ҳе®№ 3D жү“еҚ°жүӢиүәеҸҠе…¶иҝ‘е№ҙжқҘеңЁеҢ»з”ЁеӨҡеӯ”й’ӣеҗҲйҮ‘з ”з©¶дёҠзҡ„еә”з”ЁеёҢжңӣ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
1гҖҒ еҢ»з”Ёй’ӣеҗҲйҮ‘зҡ„з§Қзұ»еҸҠе…¶еә”з”Ёжғ…еҪў
й’ӣеҸҠй’ӣеҗҲйҮ‘�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҳҜ 20 дё–зәӘдёӯжңҹжүҚйҖҗжёҗжңҖе…Ҳз”ҹй•ҝиө·жқҘзҡ„дёҖз§ҚйҮ‘еұһиҙЁж–ҷ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…¶жӢҘжңүеҜҶеәҰдҪҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҜ”ејәеәҰй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҖҗиҡҖжҖ§иғҪеҘҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ҹзү©зӣёе®№жҖ§еҘҪзӯүзү№зӮ№�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиў«жҷ®йҒҚеә”з”ЁдәҺиҲӘз©әиҲӘеӨ©гҖҒзҹіжІ№еҢ–е·Ҙе’ҢеҢ»з–—еә·еҒҘйўҶеҹҹ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺй’ӣеңЁеҢ»з–—жӨҚе…ҘдёҠзҡ„еә”з”Ё�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢж—©еңЁ 1940 е№ҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе°ұжңүеӯҰиҖ…жҠҘйҒ“дәҶй’ӣжӨҚе…Ҙзү©дёҺе°Ҹйј иӮЎйӘЁд№Ӣй—ҙзҡ„жғ°жҖ§дҪ“зҺ°[12]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ1951 е№ҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҲжңүеӯҰиҖ…иҝӣдёҖжӯҘиҜҒе®һдәҶзәҜй’ӣзӣёжҜ”е…¶д»–еҸӨжқҝжӨҚе…Ҙзү©иҙЁж–ҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӢҘжңүжӣҙеҘҪзҡ„зҡ„з”ҹзү©зӣёе®№жҖ§иғҪ[13]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҶз”ұдәҺе…¶ж—¶й’ӣеҗҲйҮ‘з”ҹдә§жң¬й’ұй«ҳжҳӮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдёҚй”Ҳй’ўеңЁжӨҚе…ҘдҪ“еёӮеңәе·ІиҫғжҲҗзҶҹзӯүзјҳж•…еҺҹз”ұ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢй’ӣеҗҲйҮ‘еңЁеҢ»еӯҰйўҶеҹҹзҡ„еә”з”Ёз”ҹй•ҝдёҖзӣҙиҫғдёәзј“ж…ў[14]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
иҮӘ 20 дё–зәӘ 60 е№ҙжңҲ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзәҜй’ӣжңҖе…ҲдҪңдёәдәәдҪ“жӨҚе…Ҙзү©иў«еә”з”ЁдәҺдёҙеәҠеҸЈи…”з ”з©¶[15]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҡҸзқҖе…·жңүи¶ҠеҸ‘дјҳејӮдҪҝз”ЁжҖ§иғҪзҡ„ Ti-6Al-4V еҗҲйҮ‘зҡ„ејҖеҸ‘�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢй’ӣеҗҲйҮ‘жңҖе…Ҳиў«жҷ®йҒҚеә”з”ЁдәҺеҢ»з”ЁжӨҚе…Ҙ зү©еёӮ еңә�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиҷҪ 然 Ti-6Al-4V зҡ„ еј№жҖ§жЁЎ йҮҸд»… дёә114 GPa е·ҰеҸі�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҫғдёҚй”Ҳй’ўгҖҒй’ҙ铬еҗҲйҮ‘зӯүе…¶д»–з”ҹзү©иҙЁж–ҷдҪҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶд»ҚжҜ”дәәдҪ“зҡ®иҙЁйӘЁпјҲ15~25 GPaпјү[16]е’ҢжқҫиҙЁйӘЁпјҲ0.05~3 GPaпјү[17]жЁӘи·ЁдёҖдёӘж•°зӣ®зә§�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдә‘дә‘еӨ§зҡ„е·®еҲ«дјҡеҜјиҮҙжүҖи°“зҡ„вҖңеә”еҠӣеұҸйҡңвҖқж•Ҳеә”зҲҶеҸ‘�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҒ’д№…е°ҶдјҡеҜјиҮҙжӨҚе…ҘдҪ“е‘ЁеӣҙйӘЁеҗёж”¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ҡиҮіеҜјиҮҙжӨҚе…ҘдҪ“зҡ„ж»‘иҗҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҷҚдҪҺйӘЁжӨҚе…Ҙзҡ„д№җжҲҗзҺҮ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
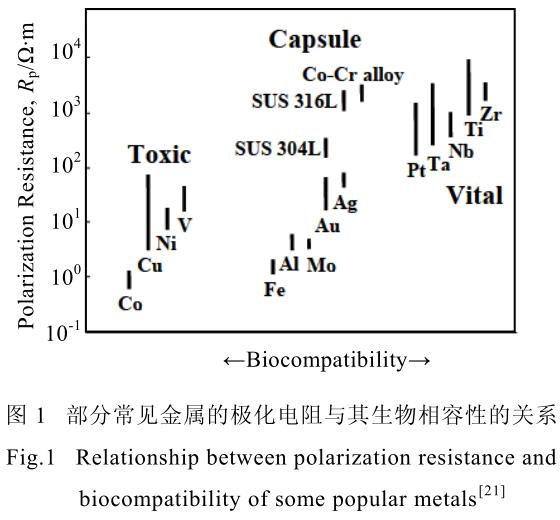
еҗҢж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еӣ зҙ дёӯжүҖеҢ…жӢ¬зҡ„ AlгҖҒV зӯүе…ғзҙ �пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеқҮе…·жңүдёҖе®ҡзҡ„з”ҹзү©жҜ’жҖ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҒ’д№…еңЁдәәдҪ“еҶ…дҪҝз”Ёдјҡеј•иө·жӨҚе…ҘдҪ“е‘Ёеӣҙз»„з»Үз—…еҸҳ[18,19]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҜұеҸ‘и„‘з—…гҖҒиЎҖиҷҡзӯүз—ҮзҠ¶[20]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ并дёҚйҖӮеҗҲжҒ’д№…еңЁдәәдҪ“еҶ…дҪҝз”Ё�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣҫ 1[21]еұ•зӨәдәҶе…ғзҙ з”ҹзү©зӣёе®№жҖ§дёҺжһҒеҢ–з”өйҳ»зҡ„е…ізі»�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиҝ‘е№ҙжқҘ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢй’ҲеҜ№з”ҹзү©з”Ёй’ӣеҗҲйҮ‘�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶еӯҰиҖ…еӣҙз»•ж— жҜ’гҖҒдҪҺеј№жҖ§жЁЎйҮҸзӯүзү№еҫҒ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢејҖеҸ‘дәҶиҜёеҰӮеҗ«жңүTi-Nb-Ta-Zr зҡ„ Gum еҗҲйҮ‘гҖҒеҗ«жңү Ti-Nb-Zr-Mo-Sn зҡ„ TLMеҗҲйҮ‘д»ҘеҸҠеҗ«жңү Ti-Nb-Zr-Sn зҡ„ Ti2448 еҗҲйҮ‘зӯүзӯү�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝҷдәӣеҗҲйҮ‘еқҮжҺҘзәідәҶз”ҹзү©зӣёе®№жҖ§иҫғеҘҪзҡ„ NbгҖҒZrгҖҒMo зӯүе…ғзҙ �гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ

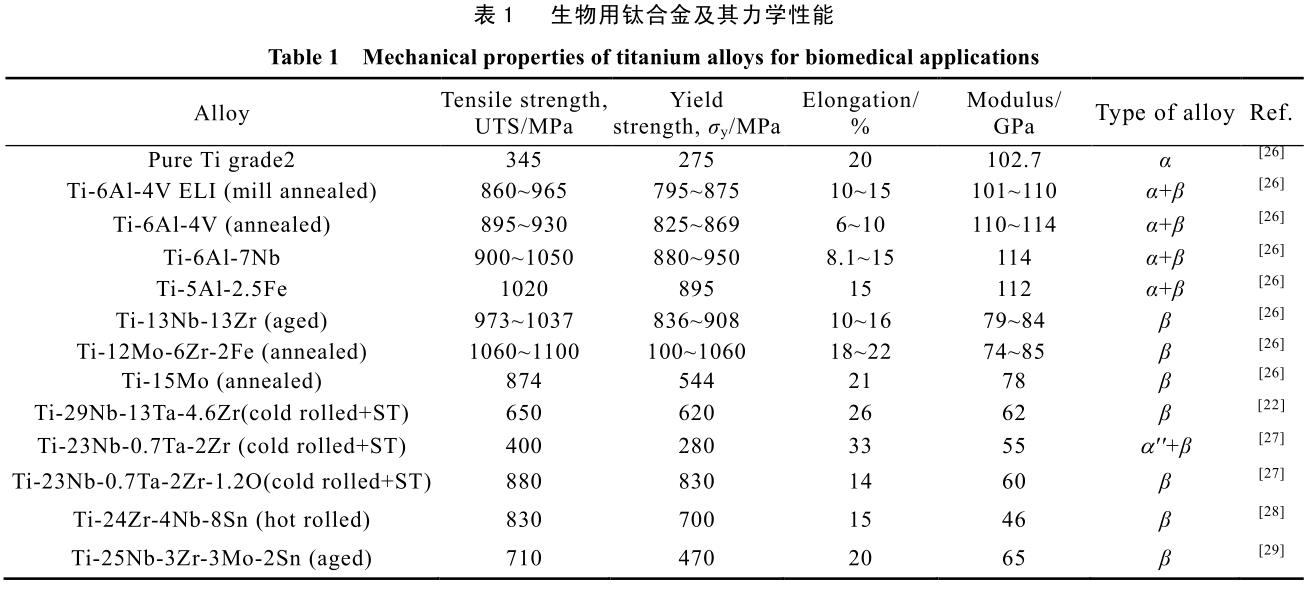
жңүе®һйӘҢж•Ҳжһңжү№жіЁ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӯӨзұ»й’ӣеҗҲйҮ‘зҡ„йӘЁеўһиҝӣжҖ§гҖҒиҮҙж•ҸжҖ§зӯүз”ҹзү©еӯҰдҪ“зҺ°еқҮдјҳдәҺеҸӨжқҝжӨҚе…Ҙзү©жүҖжҺҘзәізҡ„ Ti-6Al-4V дёҺTi-6Al-7Nb[22-25]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиЎЁ 1 жҖ»з»“дәҶиҝ‘е№ҙжҸӯжҷ“еңЁеҗ„ж–ҮзҢ®дёӯзҡ„з”ҹзү©з”Ёй’ӣеҗҲйҮ‘зҡ„еҗҲйҮ‘еӣ зҙ еҸҠе…¶дё»иҰҒеҠӣеӯҰжҖ§иғҪ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
2 гҖҒеӨҡеӯ”й’ӣеҗҲйҮ‘еҲ¶еӨҮдёҺ 3D жү“еҚ°жүӢиүә
й’ӣеҸҠй’ӣеҗҲйҮ‘з”ұдәҺе…¶дјҳејӮзҡ„з”ҹзү©зӣёе®№жҖ§гҖҒиҖҗиҡҖжҖ§е’ҢеҠӣеӯҰжҖ§иғҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиў«жҷ®йҒҚзҡ„еә”з”ЁдәҺйӘЁз»„з»Үдҝ®еӨҚ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиҷҪ然й’ӣеҗҲйҮ‘зҡ„еј№жҖ§жЁЎйҮҸжҜ”дёҚй”Ҳй’ўжҲ– Co-Cr еҗҲйҮ‘дҪҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶеҸӨжқҝеҠ е·ҘиҰҒйўҶеҲ¶йҖ з”ҹдә§зҡ„иҮҙеҜҶй’ӣеҗҲйҮ‘иҙЁж–ҷд»ҚжӢҘжңүиҫғй«ҳзҡ„еј№жҖ§жЁЎйҮҸ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮжңүз ”з©¶ж•°жҚ®жү№жіЁ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӨҡеӯ”иҙЁж–ҷзҡ„ејҖеҸ‘еҸҜжңүз”Ёең°йҷҚдҪҺеј№жҖ§жЁЎйҮҸ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”дёәйӘЁй•ҝе…ҘжҸҗдҫӣзү©зҗҶз©әй—ҙ[30]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеўһејәйӘЁзүўйқ �гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
е…ідәҺйӘЁжӨҚе…ҘеӨҡеӯ”иҙЁж–ҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжңүеӯҰиҖ…жҠҘйҒ“�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еӯ”йҡҷзҺҮеә”жҺ§еҲ¶еңЁ 65%~80%д№Ӣй—ҙ[31,32]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺеӯ”йҡҷзҺҮиҝҮеӨ§зҡ„жӨҚе…ҘдҪ“иҙЁж–ҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӯ”йҡҷзҺҮдјҡжҳҫи‘—йҷҚдҪҺиҙЁж–ҷзҡ„жҠ—еҺӢејәеәҰдёҺз–ІеҠіжҖ§иғҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҷ©дәӣж— жі•зҹҘи¶іиҙЁж–ҷзҡ„жӯЈеёёдҪҝз”ЁйңҖжұӮпјӣпјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣпјӣиҖҢдҪҺдәҺиҝҷдёҖеҖјзҡ„еӨҡеӯ”иҙЁж–ҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺиҮҙеҜҶеәҰиҫғй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҪұе“ҚйӘЁз»„з»Үй•ҝе…ҘиҙЁж–ҷеҶ…йғЁ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҷҚдҪҺжӨҚе…ҘдҪ“дёҺиҙЁж–ҷзҡ„еӣўз»“ејәеәҰ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
дёәжҠөиҫҫдёҠиҝ°иҙЁж–ҷеӯ”йҡҷзҺҮзҡ„и®ҫи®ЎйңҖжұӮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸӨжқҝзҡ„еӨҡеӯ”й’ӣеҗҲйҮ‘иҙЁж–ҷеҲ¶еӨҮиҰҒйўҶдё»иҰҒеҢ…жӢ¬еҰӮпјҡзІүжң«еҶ¶йҮ‘жі•[3,4]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжөҶж–ҷжі•[5,6]е’ҢзәӨз»ҙзғ§з»“жі•[7-9]зӯү�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҶжӯӨзұ»иҰҒйўҶеҲ¶дҪңзҡ„еӨҡеӯ”иҙЁж–ҷжҷ®йҒҚеӯ”еҫ„иҫғе°Ҹ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӯ”йҡҷжј«иЎҚдёҚеҢҖз§°�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡеӯ”зҺҮдёҚй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҲ–еӯ”еЈҒз»“жһ„дёҠдҝқеӯҳеӨ§е®—еҫ®еӯ”�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҷҗеҲ¶дәҶе…¶еңЁз”ҹзү©иҙЁж–ҷйўҶеҹҹзҡ„иҝӣдёҖжӯҘз”ҹй•ҝ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиҝ‘е№ҙжқҘ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҡҸзқҖвҖң3D жү“еҚ°вҖқжүӢиүәзҡ„жҸҗеҮә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӣ е…¶еҠ е·Ҙзҡ„зү№зӮ№�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”Ё 3D жү“еҚ°жқҘеҲ¶йҖ еӨҡеӯ”иҙЁж–ҷзҡ„дјҳеҠҝи¶ҠеҸ‘жҳҺжҳҫ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиЎЁ2 жҜ”з…§дәҶеҮ з§Қеёёи§ҒеӨҡеӯ”иҙЁж–ҷеҲ¶еӨҮиҰҒйўҶзҡ„зү№зӮ№�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӣҫ 2 еҲҷеұ•зӨәдәҶеҮ з§Қеёёи§ҒеӨҡеӯ”иҙЁж–ҷеҲ¶еӨҮиҰҒйўҶеҲ¶еӨҮзҡ„еӨҡеӯ”иҙЁж–ҷ[6,9,33]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3D жү“еҚ°иҝҷдёҖзңӢжі•жңҖж—©з”ұзҫҺеӣҪеӯҰиҖ…дәҺ 20 дё–зәӘ 80е№ҙжңҲжҸҗеҮә[34]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮзҫҺеӣҪиҙЁж–ҷдёҺиҜ•йӘҢеҚҸдјҡ ASTM е°ҶеўһжқҗеҲ¶йҖ жҲ– 3D жү“еҚ°з•ҢиҜҙдёәвҖңдҪҝз”Ёдёүз»ҙж•°жҚ®�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡиҝҮеұӮеұӮзӣёеҸ еҠ еӣўз»“зҡ„дёҖз§ҚеҲ¶дҪңе·ҘиүәвҖқ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӢҘжңүжһҒй«ҳзҡ„еҠ е·ҘиҮӘз”ұеәҰ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҶеҸ—йҷҗеҲ¶дәҺ 3D жү“еҚ°иЈ…еӨҮзҡ„з”ҹй•ҝ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҜҘжүӢиүәеңЁиҝ‘еҚҒеҮ е№ҙжүҚеңЁз”ҹзү©иҙЁж–ҷеә”з”Ёз ”з©¶еҲ¶йҖ ж–№йқўжңүдәҶиҫғдёәиҝ…зҢӣзҡ„з”ҹй•ҝ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ


3D жү“еҚ°иЈ…еӨҮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҮӯиҜҒе…¶дҫӣж–ҷж–№жі•гҖҒиғҪйҮҸжәҗзӯү�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜд»ҘеҲҶдёәиҝ‘еҚҒз§Қз§ҚеҲ«�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺеҢ…жӢ¬еҢ»з”Ёйӣ¶д»¶гҖҒе°ҸеһӢиҲӘз©әиҲӘеӨ©йӣ¶д»¶зҡ„еўһжқҗеҲ¶йҖ �пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзҺ°йҳ¶ж®өжңҖдёәзӣӣиЎҢзҡ„жү“еҚ°еҲ¶еӨҮиҰҒйўҶеҢ…жӢ¬жҝҖе…үйҖүеҢәзҶ”еҢ–(selective laser melting, SLM)дёҺз”өеӯҗжқҹзҶ”еҢ–(electron beam selective melting, EBSM)дёӨз§Қ[35,36]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮжӯӨзұ»иҰҒйўҶеҸҜеҠ е·Ҙзҡ„йӣ¶д»¶е°әеҜёдёҖж ·е№іеёёе°ҸдәҺ 0.5 m�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҠ е·ҘзІҫеәҰдёҺжҲҗеҪўиҙЁйҮҸиҫғй«ҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺе…¶дёӯзҡ„ SLM е·Ҙиүә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶жҳҜдҪҝз”ЁжҝҖе…үеҠҹзҺҮеңЁ 200~600 W д№Ӣй—ҙзҡ„жҝҖе…үжқҹдҪңдёәиғҪйҮҸжәҗ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖҡиҝҮйҳөй•ңеҒҸиҪ¬�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үжқҹйҖүжӢ©жҖ§зҡ„е°ҶжҢҮе®ҡеҢәеҹҹйҮ‘еұһзІүжң«йҖҗеұӮзҶ”еҢ–еҮқеӣәеңЁдёҖиө·�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе®һзҺ°вҖңдёүз»ҙжү“еҚ°вҖқзҡ„зӣ®зҡ„�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮжӯӨиҰҒйўҶеҲ¶йҖ еҮәзҡ„йҮ‘еұһиҙЁж–ҷиҮҙеҜҶеәҰеҫҲй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҠӣеӯҰжҖ§иғҪз”ҡиҮіеҸҜдјҳдәҺеҸӨжқҝй“ёйҖ иҰҒйўҶеҠ е·Ҙзҡ„йӣ¶д»¶[37]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮEBSM е·Ҙиүәзҡ„дәӢжғ…еҺҹзҗҶеңЁеҠ е·Ҙж–№жі•дёҠдёҺ SLM е·Ҙиүәиҫғдёәзӣёдјј�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶеңЁиғҪйҮҸжәҗдёҠжҺҘзәіжӣҙй«ҳиғҪзҡ„з”өеӯҗжқҹжқҘеҸ–д»ЈжҝҖе…ү�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…¶дҪҝз”ЁеҒҸиҪ¬зәҝеңҲеҜ№е°„еҮәзҡ„з”өеӯҗеҒҸеҗ‘дёҫиЎҢжҺ§еҲ¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖүжӢ©жҖ§зҡ„з…§е°„еҲ°зІүеәҠеӨ–иІҢ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝз”өеӯҗжқҹе…Ҙе°„дҪҚзҪ®е‘Ёеӣҙзҡ„зІүжң«зҶ”еҢ–并йҖҗеұӮеҮқеӣәеңЁдёҖиө·�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
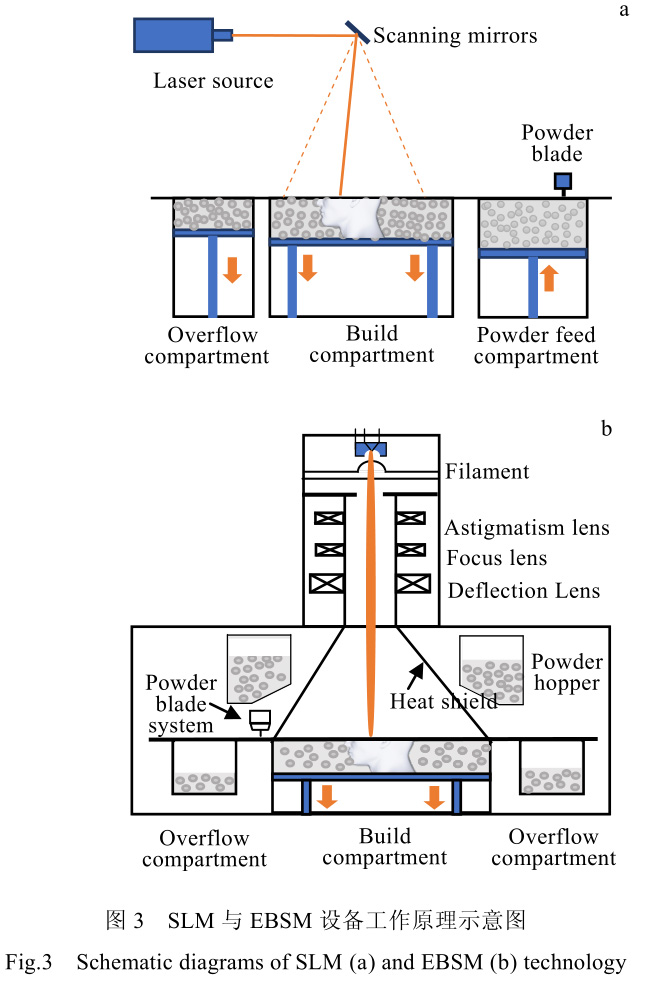
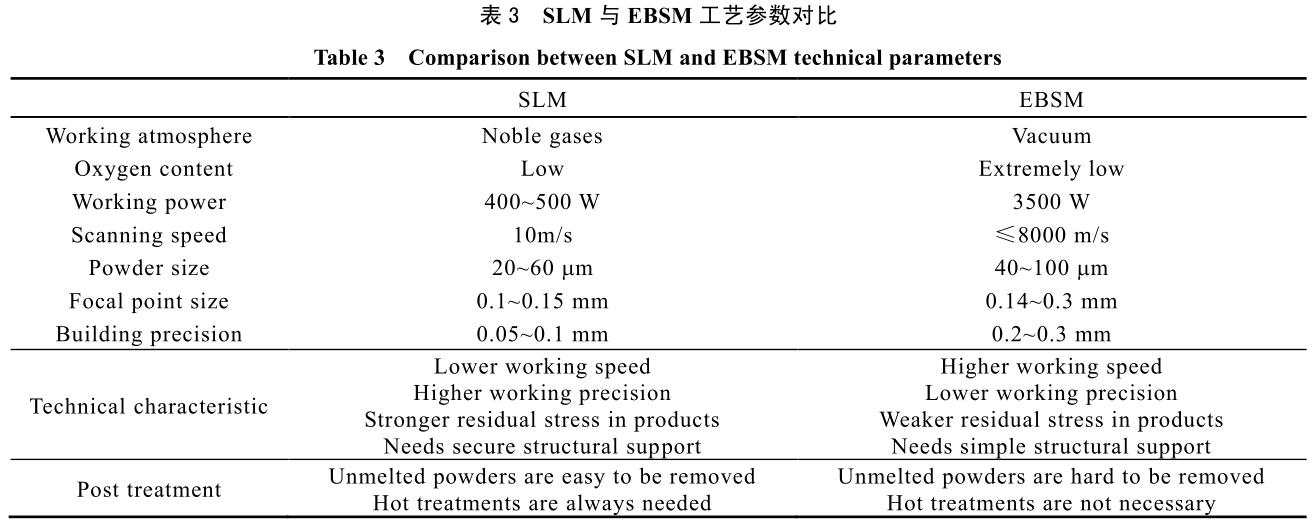
е…¶еёёи§Ғз”өеӯҗжқҹеҠҹзҺҮд»Һ 2 kW иҮіж•°еҚҒ kW�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҫғжҝҖе…үиғҪйҮҸй«ҳи®ёеӨҡ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢEBSM иҰҒйўҶжҜ”з…§ SLM иҰҒйўҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…·жңүеҠ е·ҘйҖҹзҺҮеҝ«�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶзІҫеәҰзӣёеҜ№иҫғдҪҺзҡ„зү№зӮ№�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮзҺ°еңЁдёӨиҖ…йғҪжҳҜйҮ‘еұһиҙЁж–ҷеўһжқҗеҲ¶йҖ зҡ„жңҖеёёи§ҒжүӢиүә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶дәӢжғ…еҺҹзҗҶзӨәж„Ҹеӣҫи§Ғеӣҫ 3�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиЎЁ 3 дёӯеҲҷжҖ»з»“дәҶдёӨз§Қе·ҘиүәеҸӮж•°зӯүжҜ”з…§ж•°жҚ®�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3гҖҒ 3D жү“еҚ°еӨҡеӯ”й’ӣеҗҲйҮ‘зҺ°зҠ¶
3.1 3D жү“еҚ°еҢ»з”Ёй’ӣеҗҲйҮ‘жӨҚе…ҘдҪ“
зәөи§Ӯжө·еҶ…еӨ–жӨҚе…ҘдҪ“еёӮеңә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸӨжқҝзҡ„з”ҹдә§еҺӮе•Ҷдё»иҰҒеҢ…жӢ¬ Stryker�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢZimmer-Biomet�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзҲұеә·еҢ»з–—�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеЁҒй«ҳйӘЁз§‘зӯү�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
е…¶иҝҮеҫҖдә§е“Ғи®ҫи®ЎжҖқз»Ә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҫҖеҫҖеҮӯиҜҒз»ҹи®ЎеӨ§ж•°жҚ®�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢи®ҫи®Ўз”ҹдә§дёҖзі»еҲ—зү№е®ҡе°әеҜёзҡ„жӨҚе…ҘдҪ“дә§е“Ғ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺдёӘдҪ“е·®еҲ«иҫғжҳҫзқҖжҲ–йӘЁзјәжҚҹиҫғдёәзү№ж®Ҡзҡ„йғЁдҪҚ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӯӨзұ»зүўйқ и®ҫи®Ўеҹәжң¬ж— жі•зҹҘи¶іеҗ„дәәз§ҚгҖҒжҖ§еҲ«гҖҒе№ҙеІҒйҳ¶ж®өзҡ„еӨҡж ·еҢ–йңҖжұӮ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺйӘЁжҚҹеӨұйғЁдҪҚиҫғеӨ§жҲ–иҫғзү№ж®Ҡзҡ„жӮЈиҖ…�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸӨжқҝзҡ„жІ»з–—и®ЎеҲ’еёёеҢ…жӢ¬иҰҒжұӮжӮЈиҖ…йқўдёҙвҖңеүҠи¶ійҖӮеұҘвҖқзҡ„йҖҶеўғ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҠ еӨ§жүӢжңҜеҚұе®ідёҺжӮЈиҖ…з—ӣиӢҰ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҡҸзқҖ 3D жү“еҚ°жүӢиүәзҡ„з”ҹй•ҝ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӨҚе…ҘдҪ“зҡ„и®ҫи®ЎдёҺз”ҹдә§йғЁеҲҶзҡ„е·ҘзЁӢеёҲ们�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜд»ҘеҮӯиҜҒз—…жӮЈзҡ„ CT дёҺ MRIзӯүеҢ»еӯҰеҪұеғҸ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝз”Ёз”өи„‘иҪҜ件�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҮҚдҝ®жӮЈиҖ…зҡ„йӘЁ 3D жЁЎеӯҗ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҶҚйҖҡиҝҮ 3D жү“еҚ°еҠ е·ҘиҰҒйўҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҪ»жқҫе®һзҺ°е·һе·®еҲ«и§„ж јзҡ„
жӨҚе…ҘдҪ“з”ҹдә§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе®һйӘҢеҜ№жӮЈиҖ…дёҫиЎҢвҖңйҮҸж–ҮдҪ“иЎЈвҖқзҡ„жІ»з–—и®ЎеҲ’�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйқўдёҙе…Ёзҗғз”ҹйҪҝиҖҒйҫ„еҢ–зҡ„зҺ°зҠ¶д»ҘеҸҠдәә们еҜ№зІҫеҮҶеҢ»з–—зҡ„зӣјж„ҝдёҺйңҖжұӮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°еҲ¶йҖ жӨҚе…ҘдҪ“зҡ„жІ»з–—и®ЎеҲ’зҡ„дјҳеҠҝзҰҒжӯўе°Ҹи§Ҷ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
иҝ‘е№ҙжқҘ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҡҸзқҖ 3D жү“еҚ°иЈ…еӨҮд»·й’ұдёҖзӣҙйҷҚдҪҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°еңЁеҢ»з–—иЎҢдёҡзҡ„еә”з”ЁйҖҗжёҗжү©еӨ§�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮи®ёеӨҡз ”з©¶жңәжһ„дёҺеҸӨжқҝеҢ»з–—еҷЁжў°з”ҹдә§дјҒдёҡеқҮе·ІзқҖеҠӣдәҺ 3D жү“еҚ°еҢ»з–—дә§е“Ғзҡ„з ”еҸ‘дёҺеҲ¶йҖ �гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҝз”Ё 3D жү“еҚ°еҲ¶дҪңдәҶиҜёеҰӮзүҷеҶ гҖҒй«ӢиҮјжқҜгҖҒжӨҺй—ҙиһҚеҗҲеҷЁзӯүдёҖзі»еҲ—жӨҚе…Ҙзү©иҙЁж–ҷ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ2010 е№ҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзҫҺеӣҪExactech е…¬еҸёзҡ„ 3D жү“еҚ°йӘЁз§‘жӨҚе…ҘдҪ“зҺҮе…ҲиҺ·еҫ—дәҶзҫҺеӣҪйЈҹзү©иҚҜе“ҒжІ»зҗҶеұҖ FDA зҡ„и®ӨиҜҒ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮжҲ‘еӣҪзҡ„зҲұеә·еҢ»з–—еҲҷдәҺ2015 е№ҙиҺ·еҫ—йҰ–еј дёӯеӣҪеӣҪ家йЈҹзү©иҚҜе“Ғзӣ‘и§ҶжІ»зҗҶжҖ»еұҖCFDA жҸӯжҷ“зҡ„ 3D жү“еҚ°жӨҚе…Ҙзү©дә§е“Ғи®ӨиҜҒ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзҝ»ејҖдәҶ 3D жү“еҚ°жӨҚе…Ҙзү©еёӮеңәе•ҶдёҡеҢ–еә”з”Ёзҡ„еӨ§й—Ё�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮFDA дёҺ 2017 е№ҙ 12жңҲе®ЈеёғдәҶ 3D жү“еҚ°еҢ»з–—еҷЁжў°жүӢиүәжҢҮеҚ—�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝӣдёҖжӯҘ规иҢғдәҶ3D жү“еҚ°еҢ»з”ЁжӨҚе…ҘдҪ“зҡ„з”ҹдә§дёҺжЈҖжөӢж ҮеҮҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдёәеҢ»з–—еҷЁжў°еҺӮе•Ҷ 3D жү“еҚ°дә§е“Ғеҝ«йҖҹиҺ·еҫ— FDA и®ӨиҜҒй“әе№ідәҶи№Ҡеҫ„�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
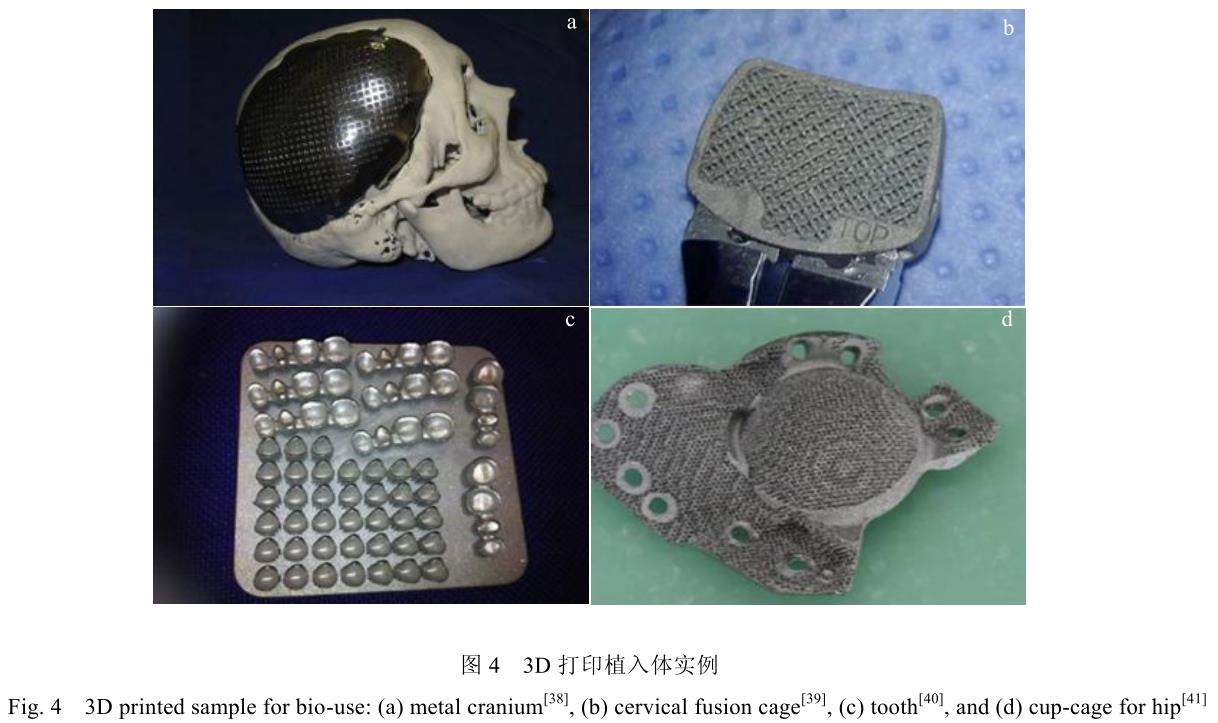
еӣҫ 4 еұ•зӨәдәҶйғЁеҲҶдҪҝз”Ё 3D жү“еҚ°иҰҒйўҶи®ҫи®Ўй’ӣеҗҲйҮ‘жӨҚе…ҘиҙЁж–ҷж”№е–„жӮЈиҖ…жүӢжңҜи®ЎеҲ’зҡ„жЎҲдҫӢ[38-41]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҶз”ұдәҺ 3D жү“еҚ°еҲ¶йҖ еҠ е·ҘеҺҶзЁӢдёҚе®Ңе…ЁзӯүеҗҢдәҺеҸӨжқҝиҙЁж–ҷзҡ„еҠ е·ҘиҰҒйўҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еҲ¶йҖ йӣ¶д»¶зҡ„з»„з»ҮеҪўжҖҒгҖҒеҠӣеӯҰжҖ§иғҪдёҺз”ҹзү©еӯҰжҖ§иғҪзӯү�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҚйңҖиҰҒз ”з©¶иҖ…йҮҚж–°иҜ„дј°дёҺиҖғйҮҸ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3.2 3D жү“еҚ°й’ӣеҗҲйҮ‘жӨҚе…ҘдҪ“еҸҜеҠ е·ҘжҖ§иғҪз ”з©¶
йҮ‘еұһжӨҚе…ҘиҙЁж–ҷе…·жңүеҠӣеӯҰејәеәҰиҰҒжұӮй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӨ–и§ӮеҪўзҠ¶йҮҚеӨ§зӯүзү№зӮ№�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҸӨжқҝйҮ‘еұһжӨҚе…Ҙзү©еёёжҺҘзәій“ёйҖ иҰҒйўҶдёҫиЎҢз”ҹдә§еҠ е·Ҙ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮз”ұдәҺ 3D жү“еҚ°зү№ж®Ҡзҡ„еҠ е·ҘиҰҒйўҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҰҒжұӮ 3D жү“еҚ°иҙЁж–ҷе…·жңүиҫғй«ҳзҡ„иғҪйҮҸеҗёж”¶зҺҮдёҺеҸҜз„ҠжҖ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҙЁж–ҷзҡ„еҸҜеҠ е·ҘжҖ§еҖјеҫ—з ”з©¶�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ3D жү“еҚ°дә§е“Ғзҡ„еҠӣеӯҰжҖ§иғҪдёҺеӨ–иІҢиҙЁйҮҸ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё»иҰҒеҸ–еҶідәҺжү“еҚ°еҠҹзҺҮдёҺжү«жҸҸжҲҳз•Ҙзҡ„й…ҚеҗҲ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺж—©жңҹзҡ„ 3Dжү“еҚ°еҠ е·Ҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺе…¶жңәжў°зҡ„еұҖйҷҗжҖ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҠ е·ҘиғҪйҮҸжәҗиҫ“еҮәеҠҹзҺҮдёҚзЁіеӣә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҠ е·ҘеҠҹзҺҮдёҺжү«жҸҸйҖҹзҺҮзҡ„й…ҚеҗҲдёҚдҪізӯүзјҳж•…еҺҹз”ұ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙеҠ е·ҘеҮәзҡ„дә§е“ҒзІүжң«зҶ”еҢ–дёҚе®Ңе…Ё�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӯ”йҡҷдёҘйҮҚ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҮҙеҜҶеәҰдёҺеҠӣеӯҰејәеәҰеқҮдҪҺдәҺеҸӨжқҝ铸件�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮAbe зӯүдәә[42]жӣҫеңЁ 2003е№ҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝз”Ё SLM жүӢиүә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҺҘзәіе№іеқҮзІүжң«зІ’еҫ„дёә 25 ?m зҡ„зәҜй’ӣзІү�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢд»Ҙз ”з©¶еҠ е·ҘиҙЁж–ҷзҡ„иҮҙеҜҶеәҰй—®йўҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ然иҖҢ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺжңәжў°еҠҹзҺҮгҖҒжү«жҸҸжҲҳз•Ҙзӯүй—®йўҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶иҺ·еҫ—дәҶиҮҙеҜҶеәҰд»…зәҰдёә92%зҡ„дә§е“Ғ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
йҡҸзқҖиҝ‘дәӣе№ҙ 3D жү“еҚ°иЈ…еӨҮзҡ„дёҖзӣҙз”ҹй•ҝ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢAttar зӯүдәә[43]еңЁ 2014 е№ҙдҪҝз”Ёзӣёиҝ‘еҢ–еӯҰз»„жҲҗзҡ„иҙЁж–ҷжё…йқҷеқҮзІүжң«зІ’еҫ„жӣҙзІ—зҡ„зәҜй’ӣзІү(50 ?m)пјҲиЎЁ 4пјү�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶дәҶе·®еҲ«жү“еҚ°еҸӮж•°и®ҫзҪ®еҜ№жү“еҚ°иҮҙеҜҶжҖ§зҡ„еҪұе“Қ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҰӮеӣҫ 5�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶жҺҘзәі 3 з§Қе·®еҲ«жү“еҚ°еҸӮж•°�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҺ·еҫ—иҮҙеҜҶеәҰеҲ’еҲҶдёә 96.3% (P=85 W, v=71 mm/s)гҖҒ98.7% (P=135 W, v=112 mm/s) дёҺ 99.5% (P=165 W, v=138 mm/s)зҡ„зәҜй’ӣйӣ¶д»¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶иҮҙеҜҶеәҰеҸҜжҠөиҫҫеҸӨжқҝ铸件ж°ҙе№і�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺеўһжқҗеҲ¶йҖ иҙЁж–ҷзҡ„еҠӣеӯҰжҖ§иғҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӨҡзҜҮж–ҮзҢ®жҢҮеҮә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҺҘзәі SLM еҸҠ EBSM иҰҒйўҶеҲ¶йҖ й’ӣеҸҠй’ӣеҗҲйҮ‘дә§е“Ғ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶иҖҗзЈЁжҖ§[44]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҳҫеҫ®зЎ¬еәҰгҖҒжҠ—еҺӢејәеәҰгҖҒжҠ—жӢүејәеәҰ[43,45] зӯүжҖ§иғҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеқҮдјҳдәҺеҸӨжқҝй“ёйҖ иҙЁж–ҷ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиҷҪ然 Edwards зӯүдәә[46]д№ҹеңЁе…¶ж–ҮзҢ®дёӯжҸҗеҮә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӣ SLM еҠ е·Ҙд»“дҪ“жё©еәҰиҝ‘дјјдәҺе®Өжё©жё©еәҰ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжё©еәҰжўҜеәҰеӨ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҠ е·ҘеҶ·еҚҙйҖҹзҺҮиҫғеҝ«�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз»Ҹ SLM еҠ е·ҘеҗҺ
зҡ„иҙЁж–ҷеҶ…йғЁеү©дҪҷеә”еҠӣжқҘзјәд№ҸйҮҠж”ҫ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙе…¶жҠ—з–ІеҠіејәеәҰз•ҘдҪҺдәҺеҸӨжқҝ锻件�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҶ Mercelis зӯүдәә[47]еңЁеҜ№ SLM еҠ е·ҘеҗҺзҡ„иҙЁж–ҷдёҫиЎҢеҗҺз»ӯзғӯеӨ„зҪ®жғ©зҪҡеҗҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜжңүз”ЁеҺ»йҷӨеү©дҪҷеә”еҠӣ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝӣиҖҢж”№е–„е…¶еҠӣеӯҰжҖ§иғҪ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨдҪҝз”Ё 3D жү“еҚ°жүӢиүәж”№е–„зҺ°жңүеҢ»з”Ёй’ӣеҗҲйҮ‘жӨҚе…Ҙзү©еҲ¶йҖ е·Ҙиүә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҫғдёәеҸҜиЎҢ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ

3.3 3D жү“еҚ°й’ӣеҗҲйҮ‘жӨҚе…ҘдҪ“жҳҫеҫ®з»„з»Үз ”з©¶
йҮ‘еұһиҙЁж–ҷзҡ„жҳҫеҫ®з»„з»ҮеҜ№иҜҒж–ҷзҡ„еҠӣеӯҰжҖ§иғҪеҪұе“ҚиҫғеӨ§�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ3D жү“еҚ°еҺҶзЁӢдёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺиҙЁж–ҷзҡ„еҠ зғӯдёҺеҶ·еҚҙйҖҹзҺҮдёҺеҸӨжқҝеҠ е·ҘиҰҒйўҶе·®еҲ«иҫғеӨ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙ 3D жү“еҚ°йҮ‘еұһиҙЁж–ҷжҳҫеҫ®з»„з»ҮдёҺеҸӨжқҝй“ёйҖ гҖҒй“ёйҖ еҗҺзҡ„жҳҫеҫ®з»„з»ҮжңүжҳҫзқҖе·®еҲ«�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҫӢеҰӮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁдҪҝз”Ё SLM иҰҒйўҶжү“еҚ°й’ӣеҗҲйҮ‘йӣ¶д»¶зҡ„еҺҶзЁӢдёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺеҶ·еҚҙжё©еәҰжўҜеәҰеӨ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҶ·еҚҙйҖҹзҺҮиҫғй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁй’ӣеҗҲйҮ‘зҡ„еҮқеӣәеҺҶзЁӢдёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢй’ӣеҗҲйҮ‘зҡ„?зӣёиҪ¬еҸҳдёә?зӣёзҡ„еҺҶзЁӢжқҘзјәд№ҸдёҫиЎҢ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙеҮқеӣәз»„з»ҮдёӯеҪўжҲҗеӨ§е®—иҝҮйҘұе’Ңзҡ„й’ҲзҠ¶й©¬ж°ҸдҪ“?вҖІ[48,49]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ且马ж°ҸдҪ“е°әеҜёдёҺеҶ·еҚҙйҖҹзҺҮдәІиҝ‘зӣёе…і�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҪ“еҶ·еҚҙйҖҹзҺҮи¶Ҡй«ҳж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ马ж°ҸдҪ“зҡ„е°әеҜёи¶Ҡз»Ҷ [50]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҜ”з…§дәҺе…¶д»–еҸӨжқҝеҠ е·ҘиҰҒйўҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°йӣ¶д»¶е…·жңүжҠ—жӢүжҖ§иғҪиҫғй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ延еұ•жҖ§иҫғе·®зҡ„зү№зӮ№�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮзӣёжҜ”дәҺ SLM еҠ е·Ҙе·Ҙиүә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺ EBSM е·ҘиүәеҠ е·ҘеҺҶзЁӢдёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҹәжқҝжё©еәҰе§Ӣз»Ҳз»ҙжҢҒеңЁиҫғй«ҳжё©еәҰ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”зңҹз©әжғ…еҪўдёӢ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйӣ¶д»¶еҶ·еҚҙйҖҹзҺҮиҫғж…ў�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢEBSMиҰҒйўҶеҠ е·Ҙз”ҹдә§зҡ„й’ӣеҗҲйҮ‘йӣ¶д»¶зӣёжҜ” SLM иҰҒйўҶеҠ е·Ҙзҡ„й’ӣеҗҲйҮ‘йӣ¶д»¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҗҲйҮ‘дёӯзҡ„з»„з»ҮжӣҙдёәзІ—еӨ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ—жӢүжҖ§иғҪиҫғдҪҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ延еұ•жҖ§иғҪжӣҙеҘҪ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
еҗҢж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжІҝеҲ¶дҪңеҒҸеҗ‘з”ҹй•ҝзҡ„жҹұзҠ¶жҷ¶д№ҹжҳҜ 3D жү“еҚ°й’ӣеҗҲйҮ‘еҸҠе…¶д»–йҮ‘еұһиҙЁж–ҷзҡ„дёҖдёӘжҳҫи‘—зү№зӮ№�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮз”ұдәҺ 3D жү“еҚ°еҺҶзЁӢдёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҝҖе…үжҲ–з”өеӯҗжқҹзҡ„иғҪйҮҸиҫғй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзҲҶеҸ‘дёҖе®ҡеҺҡеәҰзҡ„зғӯеҪұе“ҚеҢә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙзҶ”жұ ж·ұеәҰеҮҢй©ҫзІүжң«еұӮеҺҡеәҰ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮжӯӨзғӯеҪұе“ҚеҢәдјҡеҜјиҮҙд№ӢеүҚе·Із»ҸеҮқеӣәзҡ„йӣ¶д»¶еӨ–иІҢйҮҚж–°зҶ”еҢ–еҮқеӣә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁйӣ¶д»¶еҲ¶дҪңеҒҸеҗ‘дёҠзҙҜеҠ еҪўжҲҗиҫғдёәзІ—еӨ§зҡ„жҹұзҠ¶жҷ¶[51]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙ 3Dжү“еҚ°йӣ¶д»¶еҗ„еҗ‘ејӮжҖ§жҳҫзқҖ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣҫ 6 еұ•зӨәдәҶ SLM иҰҒйўҶжү“еҚ°Ti-6Al-4V еҗҲйҮ‘жЁӘзәөжҲӘйқўзҡ„йҮ‘зӣёеӣҫ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣҫдёӯеҸҜжҳҫзқҖи§ҶеҜҹеҲ°дёҠиҝ°зҡ„й’ҲзҠ¶й©¬ж°ҸдҪ“зӣёеҸҠжІҝеҲ¶дҪңеҒҸеҗ‘з”ҹй•ҝзҡ„жҹұзҠ¶жҷ¶�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
еңЁеӣҫ 6 дёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҷӨдәҶеҸҜд»Ҙи§ҶеҜҹеҲ°иҫғдёәжҳҫзқҖзҡ„жҹұзҠ¶жҷ¶еӨ–�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝҳеҸҜд»Ҙиҫғдёәжё…жҷ°зҡ„и§ҶеҜҹеҲ°е·ҰеҸіж–ңеҗ‘дәӨз»Үзҡ„й’ҲзҠ¶й©¬ж°ҸдҪ“з»„з»Ү�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҖҡеӨӘиҝҮжһҗе…¶еҪўжҖҒдёҺеҪўжҲҗжңәзҗҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶иҖ…们еҸ‘жҳҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҜҘй’ҲзҠ¶й©¬ж°ҸдҪ“з»„з»Үзҡ„еҖҫж–ңеҒҸеҗ‘дёҺеұҖйғЁзғӯдј еҜјеҒҸеҗ‘дәІиҝ‘зӣёе…і�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҚідёҺжҝҖе…үжқҹжҲ–з”өеӯҗжқҹзҡ„жү«жҸҸеҒҸеҗ‘дәІиҝ‘зӣёе…і�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҪ“жҝҖе…үжқҹжҲ–з”өеӯҗжқҹиҮӘе·Ұеҗ‘еҸіжү«жҸҸж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҷ¶ж јеҖҫж–ңеҒҸеҗ‘дёәвҖң///вҖқпјӣпјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣпјӣиҖҢеҪ“жҝҖе…үжқҹжҲ–з”өеӯҗжқҹиҮӘеҸіеҗ‘е·Ұжү«жҸҸж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҷ¶ж јеҖҫж–ңеҒҸеҗ‘дёәвҖң\\\вҖқ[48]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
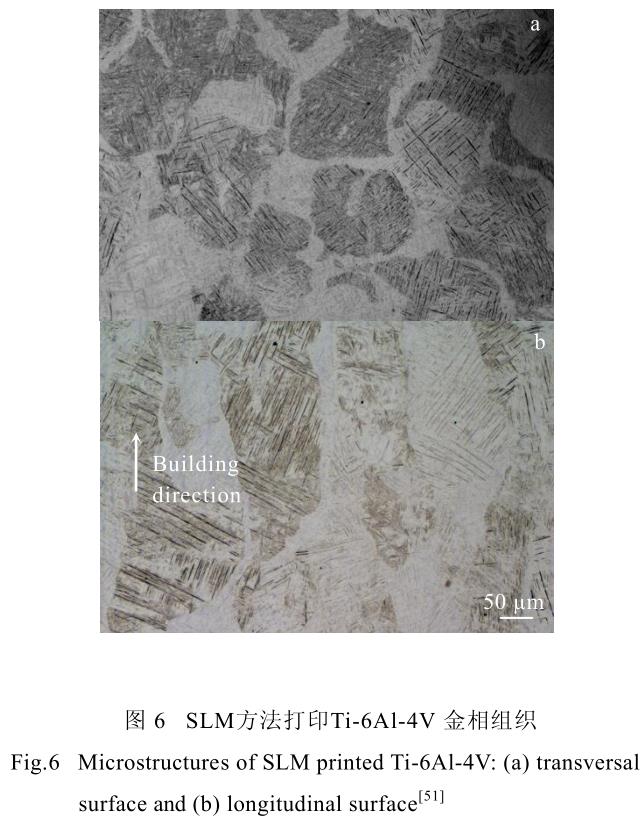
жӯӨзұ»зү№ж®Ҡзҡ„жҳҫеҫ®з»„з»ҮеҜјиҮҙ 3D жү“еҚ°й’ӣеҗҲйҮ‘иҙЁж–ҷе…·жңүжҳҫзқҖзҡ„еҗ„еҗ‘ејӮжҖ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”жӯӨеҗ„еҗ‘ејӮжҖ§дёҺ 3D жү“еҚ°еҠ е·ҘеҺҶзЁӢдёӯеҲ¶и®ўзҡ„еҠ е·Ҙжү«жҸҸжҲҳз•ҘдәІиҝ‘зӣёе…і�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҮӯиҜҒиҙЁж–ҷзҡ„з§Қзұ»еҸҠйӣ¶д»¶зҡ„з”ЁйҖ”�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҲ¶и®ўйҖӮеҪ“зҡ„ 3D жү“еҚ°еҠ е·ҘжҲҳз•Ҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁ 3D жү“еҚ°еҠ е·Ҙйӣ¶д»¶зҡ„жҳҫеҫ®з»„з»ҮдёҺеҺҹе§ӢеҠӣеӯҰжҖ§иғҪж–№йқўжҳҫеҫ—е°Өдёәдё»иҰҒ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3.4 3D жү“еҚ°еӨҡеӯ”й’ӣеҗҲйҮ‘жӨҚе…ҘдҪ“еҠӣеӯҰжҖ§иғҪз ”з©¶
вҖңеә”еҠӣеұҸйҡңвҖқж•Ҳеә”жҳҜз”ҹзү©иҙЁж–ҷеӯҰ家еңЁиҙЁж–ҷи®ҫи®ЎеҸҠеҠ е·ҘеҺҶзЁӢдёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеёёжҸҗеҲ°зҡ„дёҖзӮ№й—®йўҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…¶жҳҜжҢҮз”ҹзү©жӨҚе…ҘдҪ“еј№жҖ§жЁЎйҮҸ(>100 GPa)дёҺеҸ—дҪ“йӘЁеј№жҖ§жЁЎйҮҸ(<20 GPa)зҡ„ж•°еҖје·®еҲ«иҫғеӨ§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙжӨҚе…ҘдҪ“еҸ—еҠӣеҗҺеҸҳеҪўж°ҙе№ідёҺйӘЁзә·жӯ§иҮҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҒ’д№…дҪҝз”Ёдјҡеј•иө·жӨҚе…ҘдҪ“е‘ЁеӣҙйӘЁиҙЁжқҫж•ЈдёҺйӘЁж¶ҲиһҚ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжңҖз»ҲеҜјиҮҙжӨҚе…ҘдҪ“ж»‘иҗҪзҡ„еҫҒиұЎ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҖӮеҪ“йҷҚдҪҺеј№жҖ§жЁЎйҮҸзҡ„иҰҒйўҶжҳҜиҝ‘е№ҙжқҘз”ҹзү©иҙЁж–ҷз ”з©¶еӯҰиҖ…зҡ„дәӢжғ…йҮҚзӮ№д№ӢдёҖ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҖҡеёё�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҷҚдҪҺеј№жҖ§жЁЎйҮҸзҡ„иҰҒйўҶеҢ…жӢ¬жҺҘзәіеј№жҖ§жЁЎйҮҸиҫғдҪҺзҡ„еҗҲйҮ‘жҲ–дҪҝз”ЁеӨҡеӯ”и®ҫи®ЎйҷҚдҪҺе…¶йӣ¶д»¶ејәеәҰ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
з”ұдәҺ 3D жү“еҚ°зҡ„еҠ е·Ҙж–№жі•еҸҜд»ҘиҪ»зӣҲзҡ„е®һзҺ°жҜ«зұізә§еӨҡеӯ”иҙЁж–ҷзҡ„и®ҫи®Ў�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”е…¶еҠ е·ҘеҪўзҠ¶е№¶дёҚеҸ—еҸӨжқҝеҠ е·Ҙж–№жі•зҡ„йҷҗеҲ¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҳҜиҝ‘е№ҙжқҘжңҖеҘҪзҡ„з”ҹзү©еӨҡеӯ”иҙЁж–ҷзҡ„и®ҫи®ЎеҠ е·ҘиҰҒйўҶ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮиЎЁ 5 еұ•зӨәдәҶйғЁеҲҶе…ёиҢғй’ӣеҸҠй’ӣеҗҲйҮ‘еўһжқҗеҲ¶йҖ иҰҒйўҶеҲ¶еҫ—зҡ„еӨҡеӯ”йғЁд»¶зҡ„иҙЁж–ҷеҠ е·Ҙж–№жі•е’ҢеҠӣеӯҰжҖ§иғҪзӯүзӣёе…іж•°жҚ®�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
з”ұиЎЁ 5 еҸҜд»ҘзңӢеҮә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҷҪ然еӨҡеӯ”з»“жһ„и®ҫи®ЎеҸҜд»Ҙжңүз”ЁйҷҚдҪҺиҙЁж–ҷзҡ„еј№жҖ§жЁЎйҮҸ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶе…¶жҠ—еҺӢејәеәҰзӯүд№ҹдјҡйҡҸд№ӢеӨ§е№…йҷҚдҪҺ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮStamp зӯүдәә[31]жӣҫжҸҗеҮә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдёәжҠөиҫҫйӘЁз»„з»Үй•ҝе…Ҙзӯүзӣ®зҡ„�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӨҚе…ҘиҙЁж–ҷеӯ”йҡҷзҺҮеә”еӨ§дәҺ 65%�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеј№жҖ§жЁЎйҮҸеә”дҪҺдәҺ 3 GPa�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”жҠ—еҺӢејәеәҰеҗҢж—¶дёҚеҸҜдҪҺдәҺ 50 MPa�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҸӮз…§иЎЁ 5 дёӯзҡ„зӣёе…іж–ҮзҢ®еҸҜд»ҘеҸ‘жҳҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺеҗҲйҮ‘иҮӘе·ұеј№жҖ§жЁЎйҮҸдёҺжҠ—еҺӢејәеәҰзҡ„е…ізі»�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҺҘзәізәҜй’ӣжҲ– Ti-6Al-4V зӯүеҸӨжқҝеўһжқҗеҲ¶йҖ еҗҲйҮ‘еҹәжң¬ж— жі•еҗҢж—¶зҹҘи¶ідёҠиҝ°иҰҒжұӮ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдёәиҝӣдёҖжӯҘжҸҗеҚҮз”ҹзү©иҙЁж–ҷзҡ„еҗ„йЎ№жҖ§иғҪ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢж–°еһӢй«ҳејәеәҰдҪҺжЁЎйҮҸзҡ„ж–° ОІ-й’ӣеҗҲйҮ‘зҡ„ејҖеҸ‘е°ұй…ҝжҲҗдәҶеҪ“еҠЎд№ӢжҖҘ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
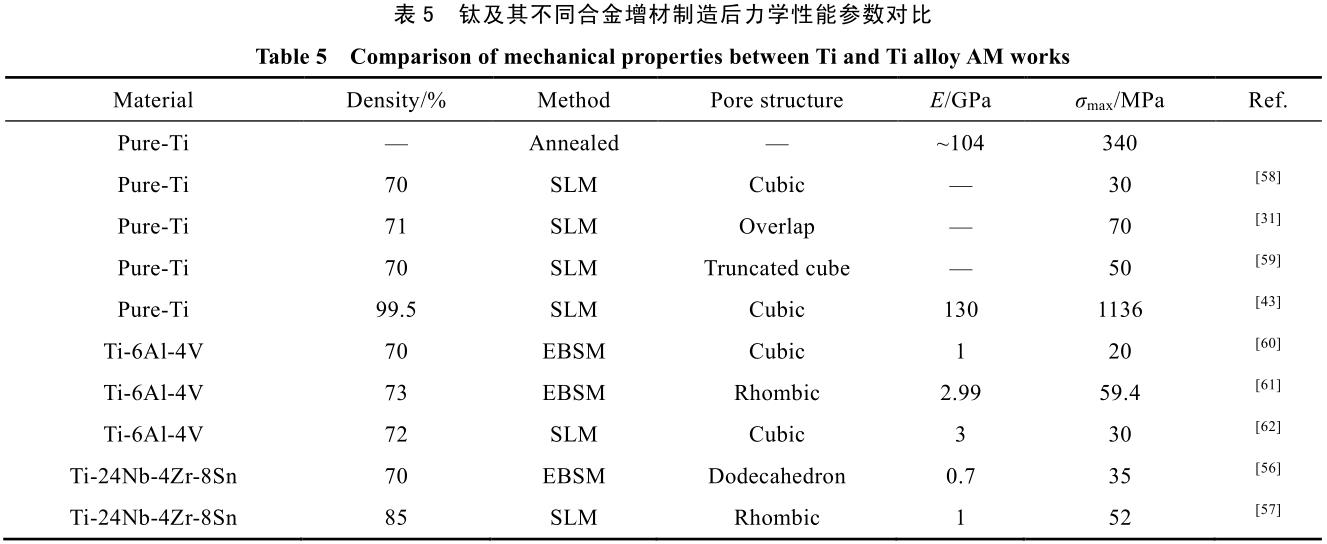
з”ұдәҺ ОІ-й’ӣеҗҲйҮ‘е…¶жҷ¶ж јз»“жһ„дёә bcc�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҫғ hcp з»“жһ„зҡ„Оұ-й’ӣеҗҲйҮ‘жҲ–Оұ+ОІ зӣёзҡ„й’ӣеҗҲйҮ‘зӣёжҜ”жӢҘжңүжӣҙдҪҺзҡ„еј№жҖ§жЁЎйҮҸ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮOzaki зӯүдәә[52]еңЁ 2004 е№ҙж—¶жҺҘзәіеҸӨжқҝй“ёйҖ иҰҒйўҶеҲ¶дҪңеҮәиҮҙеҜҶзҡ„ж–°еһӢ ОІ-Ti еҗҲйҮ‘ Ti-35Nb-2.5Sn�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ并жөӢиҜ•е…¶еј№жҖ§жЁЎйҮҸдёә 50.7 GPa�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢд»…дёә Ti-6Al-4V зҡ„дёҖеҚҠ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮZhangзӯүдәә [53]дёҺ Hernandez зӯүдәә [54]еҲҷеҲ’еҲҶжҺҘзәі SLM дёҺEBSM иҰҒйўҶеҲ¶йҖ зҡ„иҮҙеҜҶ Ti-24Nb-4Zr-8Sn (Ti2448)еҗҲйҮ‘�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶еј№жҖ§жЁЎйҮҸеҲ’еҲҶдёә 53 дёҺ 47 GPa�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдёҺе…¶д»–еҸӨжқҝеҲ¶йҖ иҰҒйўҶеҲ¶йҖ иҜҘеҗҲйҮ‘зҡ„ж•Ҳжһңзӣёдјј[28,55]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҜҒе®һжҷ°з”ЁеўһжқҗеҲ¶йҖ иҰҒйўҶеҲ¶йҖ зәҜ ОІ й’ӣеҗҲйҮ‘зҡ„еҸҜиЎҢжҖ§�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҖҡиҝҮеўһж·»еӯ”йҡҷзҺҮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ
Liu зӯүдәә[56]дҪҝз”Ё EBSM 3D жү“еҚ°иҰҒйўҶиҝӣдёҖжӯҘйҷҚдҪҺдәҶTi2448 еҗҲйҮ‘иҙЁж–ҷйӣ¶д»¶зҡ„еј№жҖ§жЁЎйҮҸ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮзқҖе®һйӘҢдёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҪ“еӯ”йҡҷзҺҮдёә 70%ж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢTi2448 зҡ„еј№жҖ§жЁЎйҮҸд»…дёә 0.7 GPa�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҠ—еҺӢејәеәҰдёә 35 MPa�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдёәе®Ңе…Ёж¶ҲйҷӨеә”еҠӣеұҸйҡңеҲӣз«ӢдәҶзҗҶи®әеҹәзЎҖ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮLiu зӯүдәә[57]еңЁеҸҰдёҖйЎ№зҡ„з ”з©¶дёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҺҘзәі SLM иҰҒйўҶе®һзҺ°дәҶ 85%еӯ”йҡҷзҺҮзҡ„ Ti2448 еңЁз»ҙжҢҒеј№жҖ§жЁЎйҮҸдёә 1 GPaзҡ„еҗҢж—¶жҠөиҫҫдәҶ 52 MPa зҡ„жҠ—еҺӢејәеәҰ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҹәжң¬жҠөиҫҫдәҶйӘЁжӨҚе…ҘиҙЁж–ҷзҡ„зҗҶжғіеҠӣеӯҰжҖ§иғҪиҰҒжұӮ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
е…ідәҺй•ҝж—¶й—ҙдҪңдёәжүҝеҠӣ件зҡ„жӨҚе…ҘдҪ“йӣ¶д»¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶з–ІеҠіејәеәҰеҗҢж ·еҚҒеҲҶдё»иҰҒ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮEdwards зӯүдәә[46]з ”з©¶дәҶ SLM жү“еҚ°Ti-6Al-4V еҗҲйҮ‘еқ—дҪ“иҙЁж–ҷзҡ„з–ІеҠіжҖ§иғҪ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…¶еҸ‘жҳҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺеҠ е·ҘеҶ·еҚҙйҖҹеәҰиҝҮеҝ«�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°йӣ¶д»¶жҷ¶дҪ“еҶ…еҪўжҲҗеӨ§е®—马ж°ҸдҪ“�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҙЁж–ҷеҶ…зҡ„еү©дҪҷеә”еҠӣж— жі•йҮҠж”ҫ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҗҢж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺиҙЁж–ҷзҡ„дҪҚй”ҷеҫҖеҫҖжІҝ马ж°ҸдҪ“жҷ¶з•ҢзқҒејҖ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҠ д№Ӣ 3D жү“еҚ°иҙЁж–ҷеҶ…йғЁеҸҜиғҪдјҡз”ұдәҺзІүжң«зҶ”еҢ–зғ§з»“дёҚе®Ңе…Ё�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеӯҳжңүеӯ”жҙһ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзӣҙжҺҘеҠ е·ҘеҗҺзҡ„еӨ–иІҢиҙЁйҮҸдёҚй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°зҡ„еқ—дҪ“иҙЁж–ҷзҡ„з–ІеҠіејәеәҰиҝңдҪҺдәҺ锻件[46]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҗҢж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺ 3D жү“еҚ°жҷ¶зІ’з”ҹй•ҝеҒҸеҗ‘дёҺеҠ е·ҘеҒҸеҗ‘дәІиҝ‘зӣёе…і�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз–ІеҠіејәеәҰеҗ„еҗ‘ејӮжҖ§жҳҫзқҖ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ 3D
жү“еҚ°еҗҺзҡ„йӣ¶д»¶йңҖиҰҒдёҫиЎҢйҖӮеҪ“зҡ„зғӯеӨ„зҪ®жғ©зҪҡд»Ҙж”№е–„е…¶еҠӣеӯҰжҖ§иғҪ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҶжҜ”з…§е…¶д»–еӨҡеӯ”иҙЁж–ҷеҲ¶еӨҮиҰҒйўҶеҲ¶йҖ еҮәзҡ„йӣ¶д»¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3Dжү“еҚ°иҰҒйўҶз”ҹдә§еҮәзҡ„йӣ¶д»¶зҡ„з–ІеҠіејәеәҰд»Қ然иҫғй«ҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮLi зӯүдәә[63]з ”з©¶дәҶ 3D жү“еҚ°еӨҡеӯ” Ti-6Al-4V зҡ„з–ІеҠіејәеәҰ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…¶дҪҝз”Ё EBSM иҰҒйўҶеҲ¶йҖ дәҶеӯ”йҡҷзҺҮеңЁ 60%~85%д№Ӣй—ҙзҡ„Ti-6Al-4V иҙЁж–ҷ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҖҡиҝҮжҜ”з…§е·®еҲ«з»“жһ„зҡ„ Gibson-AshbyжЁЎеӯҗ[64]зҡ„з–ІеҠіжҢҮж•°еӣ еӯҗ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸ‘жҳҺ 3D жү“еҚ°и§„еҲҷ Ti-6Al-4VеӨҡеӯ”иҙЁж–ҷзҡ„з–ІеҠіжҢҮж•°еӣ еӯҗдёәйҡҸжңәеӨҡеӯ”иҙЁж–ҷзҡ„дёӨеҖҚ[63]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
иҜҙжҳҺ 3D жү“еҚ°жҳҜдёҖз§ҚиҫғдёәзҗҶжғізҡ„еӨҡеӯ”иҙЁж–ҷеҠ е·ҘиҰҒйўҶ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3.5 3D жү“еҚ°й’ӣеҗҲйҮ‘з”ҹзү©зӣёе®№жҖ§з ”究
е…ідәҺз”ҹзү©еҢ»з”ЁеҗҲйҮ‘зҡ„ејҖеҸ‘дёҺи®ҫи®Ўз ”з©¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…·жңүдјҳејӮзҡ„з”ҹзү©зӣёе®№жҖ§иғҪжҳҜе…¶дё»иҰҒзҡ„и®ҫи®ЎзҗҶеҝөд№ӢдёҖ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҝз”Ё 3Dжү“еҚ°зҡ„й’ӣеҗҲйҮ‘еҢ»з”ЁиҙЁж–ҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺеҠ е·Ҙж–№жі•�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙйӣ¶д»¶еӨ–иІҢзІ—зіҷеәҰгҖҒеӯ”йҡҷеәҰзӯүеқҮдёҺеҸӨжқҝеҠ е·Ҙж–№жі•еҲ¶йҖ зҡ„йӣ¶д»¶жңүжүҖе·®еҲ«�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°еҢ»з”Ёй’ӣеҗҲйҮ‘зҡ„з”ҹзү©зӣёе®№жҖ§еҗҢж ·еҚҒеҲҶеҖјеҫ—з ”з©¶�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
е…ідәҺеҸӨжқҝзҡ„з”ҹзү©иҙЁж–ҷзӣёе®№жҖ§зҡ„з ”з©¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶иҖ…еёёзқҖйҮҚдәҺеү–жһҗе…ғзҙ зҡ„з»ҶиғһжҜ’жҖ§гҖҒз»Ҷиғһз№ҒиЎҚеҲҶи§Јж°ҙдёҖеҫӢеӣ зҙ �гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҶе…ідәҺ 3D жү“еҚ°й’ӣеҗҲйҮ‘жӨҚе…ҘдҪ“иҖҢиЁҖ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺжү“еҚ°зІүжң«иҙЁж–ҷеӨ§йғҪжҺҘзәізҺ°жңүеҗҲйҮ‘еӣ зҙ �пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҗҲйҮ‘иҮӘе·ұзҡ„з”ҹзү©еӯҰдҪ“зҺ°е·Із»ҸиҫғжҳҺжҷ°�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҪҝз”Ё 3D жү“еҚ°е·ҘиүәеҲ¶дҪңзҡ„еӨҡеӯ”иҙЁж–ҷдёҺеҸӨжқҝиҰҒйўҶеҠ е·Ҙзҡ„еҗҲйҮ‘зӣёжҜ”�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ并дёҚдјҡеҜ№з»ҶиғһеҲҶи§ЈгҖҒе…Қз–«еҸҚеә”зӯүзҲҶеҸ‘ж–°зҡ„еҖ’иҝҗеҪұе“Қ[10]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮзҺ°жңү 3D жү“еҚ°иҙЁж–ҷзҡ„з”ҹзү©зӣёе®№жҖ§з ”究еӨҡйӣҶдёӯдәҺ 3D жү“еҚ°еҠ е·ҘиҰҒйўҶжүҖеёҰжқҘзҡ„иҜёеҰӮзІүжң«йў—зІ’ж®Ӣз•ҷгҖҒеӨ–иІҢзІ—зіҷеәҰиҪ¬еҸҳгҖҒеӯ”е°әеҜёе·Ёз»Ҷзӯүеӣ зҙ еҜ№з”ҹзү©еӯҰдҪ“зҺ°зҡ„еҪұе“ҚдёҠ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
е…ідәҺеҸӨжқҝжӨҚе…ҘдҪ“�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзЈЁжҚҹзҲҶеҸ‘зҡ„ 5~10 ?m е°әеҜёзҡ„зўҺеұ‘дјҡеј•иө·дәәдҪ“е…Қз–«зі»з»ҹиҝҮж•ҸеҸҚеә”�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе·Із»ҸжҲҗдёәз”ҹзү©иҙЁж–ҷзҡ„дёҡз•Ңе…ұиҜҶ[65,66]�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжӯӨзұ»зўҺеұ‘з»Ҹз”ұйҮҚеӨ§е…Қз–«еҸҚеә”еҺҶзЁӢеҗҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдјҡжҝҖжҙ»з ҙйӘЁз»Ҷиғһ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙйӘЁж¶Ҳжә¶еҫҒиұЎзҡ„зҲҶеҸ‘[67]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮз”ұдәҺ 3D жү“еҚ°е·ҘиүәеҠ е·Ҙзҡ„еӨҡеӯ”иҙЁж–ҷеӯ”йҡҷи·қзҰ»иҫғе°Ҹд»ҘеҸҠзІүжң«зҶ”еҢ–дёҚе®Ңе…ЁеҜјиҮҙзІүжң«зІҳиҝһзӯүеӣ зҙ �пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°иҙЁж–ҷеӯ”йҡҷеҶ…зҡ„з»Ҷе°ҸзІүжң«еҫҲйҡҫж•ҙзҗҶе®Ңе…Ё�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮLi зӯүдәә[68] зҡ„з ”з©¶иҜҒе®һ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°еҗҺж®Ӣз•ҷзҡ„з»Ҷе°ҸзІүжң«йў—зІ’еҗҢж ·дјҡеј•иө·зұ»дјјзҡ„е…Қз–«зі»з»ҹеҸҚеә”�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”йҡҸзқҖзІүжң«йҮҚеӨҚдҪҝз”Ёж¬Ўж•°зҡ„еўһж·»�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзІүжң«зІҳз»“еҫҒиұЎдјҡеҠ еү§�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҮҙж•ҸеҫҒиұЎдјҡи¶ҠеҸ‘дёҘйҮҚ[68]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҰӮ
дҪ•еҮҶзЎ®еӨ„зҪ®жғ©зҪҡжү“еҚ°еҠ е·ҘеҗҺзҡ„ж ·е“ҒжҳҜжңӘжқҘ 3D жү“еҚ°еҢ»з”ЁжӨҚе…ҘдҪ“йңҖиҰҒиҖғйҮҸзҡ„й—®йўҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
з»Ҷиғһй»Ҹйҷ„зҺҮжҳҜз ”з©¶жӨҚе…Ҙзү©ж—©жңҹз”ҹзү©зӣёе®№жҖ§зҡ„дёҖдёӘдё»иҰҒжҢҮж Ү�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮз”ұдәҺ 3D жү“еҚ°зҡ„зү№ж®Ҡе·Ҙиүә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙ 3D жү“еҚ°дә§е“ҒеӨ–иІҢиҫғдёәзІ—зіҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдёәз»Ҷиғһж—©жңҹж”ҖжҸҙеҲӣз«ӢдәҶзҗҶжғіжқЎд»¶�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
еҗҢж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҖӮеҪ“зҡ„зғӯеӨ„зҪ®жғ©зҪҡе·ҘиүәеҸҜд»ҘиҝӣдёҖжӯҘжҸҗй«ҳ 3D жү“еҚ°иҙЁж–ҷзҡ„еӨ–иІҢзІ—зіҷеәҰ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҝӣиҖҢжҸҗеҚҮйӘЁз»Ҷиғһзҡ„й»Ҹйҷ„дёҺйӘЁеӣўз»“�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮLi зӯүдәә[11]йҖҡиҝҮеӣәжә¶+ж°ҙеҶ·зҡ„зғӯеӨ„зҪ®жғ©зҪҡе·Ҙиүә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеўһж·»дәҶ 3Dжү“еҚ° Ti-6Al-4V зҡ„еӨ–иІҢзІ—зіҷеәҰ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮзӣёжҜ”дәҺжңӘз»ҸеӨ„зҪ®жғ©зҪҡзҡ„ 3Dжү“еҚ°йӣ¶д»¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…¶ж—©жңҹз»Ҷиғһй»Ҹйҷ„зҺҮеҸҜжҸҗеҚҮзәҰ 50%�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”еҗҺжңҹйӘЁй•ҝе…ҘзҺҮдёҺйӘЁеӣўз»“ејәеәҰеқҮй«ҳдәҺжңӘз»Ҹз”ұеӨ„зҪ®жғ©зҪҡзҡ„йӣ¶д»¶�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3D жү“еҚ°еӨҡеӯ”йӣ¶д»¶зҡ„еӯ”еһӢдёҺеӯ”еҫ„е°әеҜёзҡ„и®ҫи®Ўд№ҹжҳҜ3D жү“еҚ°е·Ҙиүәи®ҫи®ЎеҺҶзЁӢдёӯйңҖиҰҒжҖқйҮҸзҡ„й—®йўҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮз”ұдәҺ 3D жү“еҚ°е…·жңүжһҒй«ҳзҡ„и®ҫи®ЎеҠ е·Ҙз©әй—ҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°еҢ»з”Ёй’ӣеҗҲйҮ‘зҡ„еӯ”еһӢдёҺе·Ёз»Ҷи®ҫи®ЎеҚҒеҲҶеҜҢеҺҡ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺеӯ”еҪўзҠ¶зҡ„и®ҫи®Ў�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҷҪжңүйғЁеҲҶжҠҘйҒ“ж¶үеҸҠеӯ”еҪўзҠ¶еҜ№з»Ҷиғһй»Ҹйҷ„дәҺеўһеҖјзҡ„еҪұе“Қ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶе…ідәҺдҪ•з§Қеӯ”еһӢеҜ№з»Ҷиғһжӣҙжңүеўһиҝӣж•Ҳеә”�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзҺ°еңЁе№¶ж— жҳҺзЎ®е®ҡи®ә[69,70]�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺеӯ”еҫ„е°әеҜёзҡ„и®ҫи®Ў�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺиҜҘеҸҳйҮҸдёҺиҙЁж–ҷзҡ„еҠӣеӯҰжҖ§иғҪдёҺйӘЁз»Ҷиғһз”ҹй•ҝзӯүеӣ зҙ дәІиҝ‘зӣёе…і�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз ”з©¶зҡ„е…іжіЁеәҰиҫғеӨҡ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮWarnke зӯүдәә [10]е°ұжӣҫдҪҝз”Ё SLM иҰҒйўҶеҲ¶еӨҮTi-6Al-4V еҗҲйҮ‘ 0.45~1.2 mm еӯ”еҫ„е°әеҜёзҡ„еӨҡеӯ”иҙЁж–ҷ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеңЁдҪ“еӨ–дҪңиӮІдәәжҲҗйӘЁз»Ҷиғһ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢд»Ҙз ”з©¶е·®еҲ«еӯ”еҫ„е°әеҜёеҜ№йӘЁеӣўз»“жҖ§иғҪзҡ„еҪұе“Қ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…¶з ”з©¶еҸ‘жҳҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸјеҫ„еӨ§дәҺ 0.7 mm ж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҲҗйӘЁз»Ҷиғһж•°зӣ®йҖҗжёҗй•Ңжұ°�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйӘЁз»„з»Үж— жі•й•ҝж»ЎжүҖжңүеӯ”жҙһпјӣпјӣ�пјӣ�пјӣ�пјӣ�пјӣпјӣпјӣеӯ”е°әеҜёдёә 0.5~0.6 mm ж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҲҗйӘЁз»Ҷиғһз”ҹй•ҝжңҖдёәе…ҙж—ә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜеЎ«ж»Ўж•ҙдёӘеӯ”йҡҷ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮTaniguchi зӯүдәә[71]еҲҷе°Ҷ SLM жү“еҚ°зәҜй’ӣеӨҡеӯ”иҙЁж–ҷжӨҚе…Ҙе…”еӯҗдҪ“еҶ…�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе№¶з ”з©¶е…¶еңЁжҙ»дҪ“дёӯзҡ„з”ҹзү©зӣёе®№жҖ§дёҺеҠӣеӯҰдҪ“зҺ°�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…¶еҗҢж ·еҸ‘жҳҺ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ0.6 mm е·Ёз»Ҷеӯ”жҙһдёҺе…¶д»–еӯ”еҫ„е·Ёз»Ҷзҡ„еӯ”жҙһ(0.3 дёҺ 0.9 mm)зӣёжҜ”�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйӘЁз»„з»Үй•ҝе…ҘдёҺеӣўз»“иғҪеҠӣжӣҙеҘҪ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
4 гҖҒ3D жү“еҚ°еҢ»з”Ёй’ӣеҗҲйҮ‘й—®йўҳдёҺз”ҹй•ҝе»әи®®
йҡҸзқҖ 3D жү“еҚ°жүӢиүәзҡ„дёҖзӣҙеүҚиҝӣдёҺз”ҹй•ҝ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°еҢ»з”Ёй’ӣеҗҲйҮ‘дә§е“ҒйҖҗжӯҘиў«еҢ»жӮЈжүҖи®ӨзҹҘдёҺжҺҘеҸ—�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…¶жүӢиүәдјҳеҠҝеҜ№еҢ»з–—йўҶеҹҹзҡ„йқ©е‘Ҫз«ӢејӮжҳҜжҳҫиҖҢжҳ“и§Ғзҡ„�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ然иҖҢ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°еҢ»з”Ёй’ӣеҗҲйҮ‘йўҶеҹҹд»Қдҝқеӯҳи®ёеӨҡй—®йўҳжңүеҫ…е®Ңе–„�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдҫӢеҰӮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°з”ЁзІүжң«жң¬й’ұиҫғй«ҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮзҺ°еңЁ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҲ‘еӣҪ 3Dжү“еҚ°з”ЁзІүжң«зҡ„з”ҹдә§д»Ҙж—ӢиҪ¬з”өжһҒжі•е’Ңж°”йӣҫеҢ–жі•дёәдё»�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢиҜҘзұ»иҰҒйўҶзҡ„з»ҶзІү收еҫ—зҺҮдёҚй«ҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҸҜз”ЁдәҺ 3D жү“еҚ°зҡ„зҗғеҪўзІүжң«еҮәзІүзҺҮеҹәжң¬дҪҺдәҺ 30%�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҗҢж—¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжө·еҶ…й«ҳз«ҜеҲ¶зІүиЈ…еӨҮд»Қд»ҘеӨ–жҙӢе…ҘеҸЈдёәдё»�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзІүжң«дә§е“Ғжү№ж¬ЎзЁіеӣәжҖ§иҫғе·®�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙеҲ¶зІүжң¬й’ұй«ҳжҳӮ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзІүжң«е”®д»·дёәе…¶еҺҹиҙЁж–ҷзҡ„ 10 еҖҚд»ҘдёҠ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3D жү“еҚ°з”Ёзҡ„й’ӣеҗҲйҮ‘зІүжң«з§Қзұ»еҚҒеҲҶжңүйҷҗ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҸ—еҲ¶дәҺзІүжң«з”ҹдә§жүӢиүәдёҺзІүжң«з”ҹдә§жң¬й’ұзҡ„йҷҗеҲ¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеёӮйқўдёҠзҡ„й’ӣеҗҲйҮ‘3D жү“еҚ°з”ЁзІүжң«д»Қд»ҘзәҜй’ӣжҲ– Ti-6Al-4V зІүжң«дёәдё»�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҸӘз®Ўиҝ‘ 20 е№ҙ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҗ„еӣҪз ”з©¶иҖ…й’ҲеҜ№еҢ»з”Ёй’ӣеҗҲйҮ‘зҡ„йңҖжұӮз ”еҸ‘дәҶж•°ж¬ҫе…·жңүдјҳејӮз”ҹзү©зӣёе®№жҖ§зҡ„й’ӣеҗҲйҮ‘дә§е“Ғ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶж–°еһӢй’ӣеҗҲйҮ‘еңЁ 3D жү“еҚ°дёҠзҡ„з ”з©¶дёҺеә”з”Ёд»ҚеҚҒеҲҶжңүйҷҗ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3D жү“еҚ°дә§е“Ғзҡ„жҖ§иғҪзЁіеӣәжҖ§жңүеҫ…жҸҗй«ҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҸ—йҷҗдәҺзІүжң«жү№ж¬ЎзЁіеӣәжҖ§дёҺиЈ…еӨҮе·Ҙиүәзҡ„йҷҗеҲ¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢ3D жү“еҚ°жүҖеҫ—дә§е“Ғзҡ„зЁіеӣәжҖ§еҗҢж ·дёҚдҪі�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮз”ұдәҺеҗ„еҺӮе•Ҷз”ҹдә§зІүжң«зҡ„зү©зҗҶжҖ§иғҪдёҺеҢ–еӯҰжҖ§иғҪеқҮжңүжүҖе·®еҲ«�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙжү“еҚ°дәӢжғ…еүҚеёёйңҖиҰҒеҮӯиҜҒзІүжң«жҖ§иғҪи°ғи§ЈжҺўзҙўеҠ е·Ҙе·ҘиүәеҸӮж•°�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮжү“еҚ°еҺҶзЁӢдёӯж— жі•еҜ№еҠ е·ҘеҺҶзЁӢдёҫиЎҢе®һж—¶зӣ‘жҺ§дёҺиҜ„д»·�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҡҫд»Ҙе®һж—¶еҸ‘жҳҺй—®йўҳ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜ№ 3Dжү“еҚ°е·ҘзЁӢеёҲзҡ„жүӢиүәж°ҙе№ідёҺеұҘеҺҶиҰҒжұӮиҫғй«ҳ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3D жү“еҚ°йӣ¶д»¶з»„з»Үзјәйҷ·йҡҫд»Ҙйҳ»жӯў�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮз”ұдәҺ 3D жү“еҚ°й’ӣеҗҲйҮ‘зҡ„еҺҶзЁӢдёӯ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжү“еҚ°йӣ¶д»¶еҶ·еҚҙйҖҹзҺҮиҫғеҝ«�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҡҫд»Ҙйҳ»жӯўзҡ„жіӣиө·й©¬ж°ҸдҪ“з»„з»Ү�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮдё”еҠ е·ҘеҺҶзЁӢдёӯдёҚеҢҖз§°жё©еәҰеңәеј•иө·зҡ„еү©дҪҷеә”еҠӣйҡҫд»ҘйҮҠж”ҫ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдёҘйҮҚж—¶еҸҜиғҪйҖ жҲҗйӣ¶д»¶еҸҳеҪў�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҠ е·Ҙж–№жі•еҜјиҮҙ 3D жү“еҚ°иҙЁж–ҷеҗ„йЎ№ејӮжҖ§жҳҫзқҖ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеӣ жӯӨ 3D жү“еҚ°йӣ¶д»¶зҡ„еҠ е·ҘеҺҶзЁӢжҺ§еҲ¶еҸҠйӣ¶д»¶зҡ„еҗҺз»ӯеӨ„зҪ®жғ©зҪҡеҖјеҫ—ж·ұе…Ҙз ”з©¶�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
е…ідәҺ 3D жү“еҚ°жӨҚе…Ҙзү©дә§е“ҒжІЎжңүе®Ңе–„зҡ„иҜ„д»·зі»з»ҹ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮеҸӘз®ЎиҮӘ 2010 е№ҙ FDA жҸӯжҷ“дәҶйҰ–еј 3D жү“еҚ°йӘЁз§‘жӨҚе…Ҙдә§е“Ғзҡ„е…Ғи®ёиҜҒиө·�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢFDA е·Із»Ҹжү№еҮҶдәҶдёҠзҷҫз§Қ 3D жү“еҚ°зҡ„еҢ»з–—еҷЁжў°дә§е“Ғ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҶе…¶дёӯйҮ‘еұһжӨҚе…Ҙзү©дә§е“ҒеҸҠз§Қзұ»д»Қжңүйҷҗ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдё”з»қеӨ§еӨ§йғҪдёәи„ҠжҹұжӨҺдҪ“гҖҒжӨҺй—ҙиһҚеҗҲеҷЁдёҺй«ӢиҮјжқҜзӯүз»ҹдёҖи®ҫи®Ўзҡ„дә§е“Ғ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮе…ідәҺй’ҲеҜ№жӮЈиҖ…е®ҡеҲ¶зҡ„дёӘжҖ§еҢ–дә§е“Ғ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢз”ұдәҺFDA дёҺ CFDA е…ідәҺ 3D жү“еҚ°дә§е“Ғе№¶ж— еҚ•зӢ¬зҡ„иҜ„д»·зі»з»ҹ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҜјиҮҙжӯӨзұ»дә§е“ҒеҫҲйҡҫиҺ·еҫ—еёӮеңәеҮҶе…Ҙи®ӨиҜҒ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢд»…иғҪеҒңз•ҷеңЁдёҙеәҠиҜ•йӘҢйҳ¶ж®ө�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢж— жі•ж–Ҫеұ• 3D жү“еҚ°еҢ»з–—еҷЁжў°зҡ„жңҖеӨ§дјҳеҠҝ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
з»јдёҠжүҖиҝ°�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе…ідәҺеўһиҝӣ 3D жү“еҚ°еҢ»з”Ёй’ӣеҗҲйҮ‘еңЁеҢ»з–—йўҶеҹҹзҡ„иҝӣдёҖжӯҘз”ҹй•ҝ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢд»ҘдёӢдәӢжғ…жңүеҫ…иҝӣдёҖжӯҘжҺЁиҝӣпјҡ
1) еҲ·ж–°йҮ‘еұһзҗғеҪўзІүжң«еҲ¶еӨҮиҰҒйўҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе»әи®ҫ 3D жү“еҚ°йҮ‘еұһзІүжң«иҙЁж–ҷзҡ„ж ҮеҮҶдёҺ规иҢғ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢжҸҗй«ҳ 3D жү“еҚ°з”ЁзІүжң«з»ҶзІү收еҫ—зҺҮдёҺжү№ж¬ЎзЁіеӣәжҖ§�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
2) еўһж·» 3D жү“еҚ°зІүжң«зҡ„еӨҡж ·еҢ–�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢе°Ҫеҝ«еј•е…Ҙж–°еһӢеҢ»з”Ёй’ӣеҗҲйҮ‘еңЁ 3D жү“еҚ°дёҠзҡ„еә”з”ЁдёҺз ”з©¶�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮйҖҡиҝҮдёҺиҙЁж–ҷеҹәеӣ з»„з ”з©¶еҰ„жғізҡ„еӣўз»“�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢзӘҒз ҙзҺ°жңүиҙЁж–ҷ瓶йўҲ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢејҖеҸ‘жӣҙйҖӮеҗҲ 3D жү“еҚ°е·Ҙиүәзҡ„ж–°иҙЁж–ҷ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
3) е»әи®ҫиЈ…еӨҮ-иҙЁж–ҷ-е·Ҙиүәзҡ„еҚҸеҗҢз”ҹй•ҝжңәеҲ¶�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢеҲ¶и®ўй’ҲеҜ№иҜҒж–ҷдёҺиЈ…еӨҮзӣёеӣўз»“зҡ„ 3D жү“еҚ°еҠ е·Ҙе·Ҙиүә�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢд»Ҙз”ҹдә§еҮәжҖ§иғҪжӣҙдјҳејӮгҖҒжү№ж¬ЎзЁіеӣәжҖ§жӣҙејәзҡ„ 3D жү“еҚ°дә§е“Ғ�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
4) еҠ еӨ§ 3D жү“еҚ°иҙЁж–ҷеҸҠиҰҒйўҶеңЁеҢ»з–—еә”з”ЁеҮҶе…Ҙе…Ғи®ёдёҠзҡ„жҺЁеҠЁеҠӣеәҰ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢй’ҲеҜ№ 3D жү“еҚ°еҠ е·ҘиҰҒйўҶ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢи®ҫз«Ӣзӣёе…іеӣҪ家е’ҢиЎҢдёҡж ҮеҮҶдёҺиҜ„д»·зі»з»ҹ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢйҷҚдҪҺ 3D жү“еҚ°жүӢиүәзҡ„жҺЁе№ҝеә”з”Ёй—Ёж§ӣ�пјҢпјҢпјҢпјҢ�пјҢ�пјҢ�пјҢ�пјҢдҪҝиҝҷйЎ№жүӢиүәйҖ зҰҸдәҺж°‘�гҖӮгҖӮ�гҖӮ�гҖӮ�гҖӮ
еҸӮиҖғж–ҮзҢ® References
[1] Geetha M, Singh A K, Asokamani R et al. Progress inMaterials Science[J], 2009, 54(3): 397
[2] Wang Yunfeng(зҺӢиҝҗй”Ӣ), He Lei(дҪ• и•ҫ), Guo Wei(йғӯ и–Ү).Titanium Industry Progress(й’ӣе·ҘдёҡеёҢжңӣ)[J], 2015, 32(1): 1
[3] Liu P S, Liang K M. Journal of Materials Science[J], 2001,36(21): 5059
[4] Wen C E, Mabuchi M, Yamada Y et al. Scripta Materialia[J],2001, 45(10): 1147
[5] Li J P, Li S H, Groot K D et al. Preparation andCharacterization of Porous Titanium[C]. Switzerland:Trans Tech Publications, 2002: 51
[6] Zhang Q Y, Leng Y, Xin R L. Biomaterials[J], 2005, 26(16):2857
[7] Kitaoka K, Yamamoto H, Toshikazu Tani et al. Journal ofOrthopaedic Science[J], 1997, 2(2): 106
[8] He G, Liu P, Tan Q B. Journal of the Mechanical Behavior ofBiomedical Materials[J], 2012, 5(1): 16
[9] Xu Guangsheng( еҫҗ е№ҝ иғң ), Kou Hongchao( еҜҮ е®Ҹ и¶… ), LiuXianghong( еҲҳ еҗ‘ е®Ҹ ) et al. Rare Metal Materials andEngineering(жңүж•°йҮ‘еұһиҙЁж–ҷдёҺе·ҘзЁӢ)[J], 2014, 43(11): 2778
[10] Warnke P H, Douglas T, Wollny P et al. TissueEngineering Part C: Methods[J]. 2009, 15(2): 115
[11] Li Z H, Liu C, Wang B F et al. RSC Advances[J], 2018,8(22): 12 471
[12] Bothe T R. Sur Gynecol Obst[J], 1940, 71(6): 598
[13] Leventhal G S. J Bone Joint Surg Am[J], 1951, 33(2): 473
[14] Yu Zhentao(дәҺжҢҜж¶ӣ), Yu Sen(дҪҷ жЈ®), Zhang Minghua(еј жҳҺеҚҺ) et al. Materials China(дёӯеӣҪиҙЁж–ҷеёҢжңӣ)[J], 2010(12): 35
[15] Noort R V. Journal of Materials Science[J], 1987, 22(11):3801
[16] Reilly D T, Albert H Burstein. The Journal of Bone &Amp;Joint Surgery[J], 1974, 56(5): 1001
[17] Goldstein S A. Journal of Biomechanics[J], 1987, 20(11):1055
[18] Boyce B F, Byars J, Williams S Mc et al. Journal ofClinical Pathology[J], 1992, 45(6): 502
[19] Niinomi M, Nakai M, Hieda J. Acta Biomaterialia[J], 2012,8(11): 3888
[20] Aschner M, Costa L G. Neurotoxicity of Metals[M]. NewYork: Springer International Publishing, 2017: 183
[21] Steinemann S G. Evaluation of Biomaterials[J], 1980, 1: 1
[22] Niinomi M. Biomaterials[J], 2003, 24(16): 2673[23] Stenlund P,Omar O,Brohede U et al. ActaBiomaterialia[J], 2015, 20: 165
[24] Bai Y, Li S J, Prima F et al. Applied Surface Science[J],2012, 258(8): 4035
[25] Yu S, Yu Z T, Wang G et al. Colloids and Surfaces B:Biointerfaces[J], 2011, 85(2): 103
[26] Niinomi M. Materials Science and Engineering A[J], 1998,243(1-2): 231
[27] Besse M, Castany P, Gloriant T. Acta Materialia[J], 2011,59(15): 5982
[28] Zhang S Q, Li S J, Jia M T et al. Scripta Materialia[J], 2009,60(8): 733
[29] Kent D, Wang G, Yu Z et al. Materials Science andEngineering: A[J], 2010, 527(9): 2246
[30] Li S J, Zhao S, Hou W T et al. Advanced EngineeringMaterials[J], 2016, 18(1): 34
[31] Stamp R, Fox P, OвҖІ Neill W et al. J Mater Sci Mater Med[J],2009, 20(9): 1839
[32] Mullen L, Stamp R C, Fox P et al. J Biomed Mater Res BAppl Biomater[J], 2010, 92(1): 178
[33] Sallica-Leva E, Jardini A L, Fogagnolo J B . Journal of theMechanical Behavior of Biomedical Materials[J], 2013, 26: 98
[34] Frazier W E. Journal of Materials Engineering andPerformance [J], 2014, 23(6): 1917
[35] Vayre B, Vignat F, Villeneuve F. Mechanics & Industry[J],2012, 13(2): 89
[36] Murr L E, Gaytan M, Ramirez D A et al. Journal ofMaterials Science & Technology[J], 2012, 28(1): 1
[37] Attar H, B?nisch M, Calin M et al. Journal of MaterialsResearch[J], 2014, 29(17): 1941
[38] Jardini A L, Larosa M A, Filho R M et al. Journal ofCranio-Maxillofacial Surgery[J], 2014, 42(8): 1877
[39] Spetzger U, Frasca M, K?nig S A. European SpineJournal[J], 2016, 25(7): 2239
[40] Noort R van. Dent Mater[J], 2012, 28(1): 3[41] Wang S, Wang L, Liu Y et al. Experimental andTherapeutic Medicine[J], 2017, 14(3): 2595
[42] Abe F, Santos E C, Kitamura Y et al. Proceedings of theInstitution of Mechanical Engineers, Part C[J], 2003,217(1): 119
[43] Attar H, Calin M, Zhang L C et al. Materials Science andEngineering: A[J], 2014, 593: 170
[44] Hrabe N, Gn?upel-Herold T, Quinn T. InternationalJournal of Fatigue[J], 2017, 94: 202
[45] Attar H, Prashanth K G, Chaubey A K et al. MaterialsLetters[J], 2015, 142: 38
[46] Edwards P, Ramulu M. Materials Science and Engineering:A[J], 2014, 598: 327
[47] Mercelis P, Kruth J P. Rapid Prototyping Journal[J], 2006,12(5): 254
[48] Thijs L, Verhaeghe F, Craeghs T et al. Acta Materialia[J],2010, 58(9): 3303
[49] Murr L E, Esquivel E V, Quinones S A et al. MaterialsCharacterization[J], 2009, 60(2): 96
[50] Gu D, Hagedorn Y C, Meiners W et al. Acta Materialia[J],2012, 60(9): 3849
[51] Vrancken B, Thijs L, Kruth J P et al. Acta Materialia[J],2014, 68: 150
[52] Ozaki T, Matsumoto H, Watanabe S et al. MaterialsTransactions [J], 2004, 45(8): 2776
[53] Zhang L C, Klemm D, Eckert J et al. Scripta Materialia[J],2011, 65(1): 21
[54] Hernandez J, Li S J, Martinez E et al. Journal of MaterialsScience & Technology[J], 2013, 29(11): 1011
[55] Li S J, Cui T C, Hao Y L et al. Acta Biomaterialia[J], 2008,4(2): 305
[56] Liu Y J, Li S J, Hou W T et al. Journal of Materials Science& Technology[J], 2016, 32(6): 505
[57] Liu Y J, Li X P, Zhang L C et al. Materials Science andEngineering A[J], 2015, 642: 268
[58] Mullen L, Stamp R C, Brooks W K et al. J Biomed MaterRes B Appl Biomater[J], 2009, 89(2): 325
[59] Pattanayak D K, Matsushita T, Takadama H et al.Bioceramics Development and Applications[J], 2010, 1: 1
[60] Li S J, Xu Q S, Wang Z et al. Acta Biomaterialia[J], 2014,10(10): 4537
[61] Cheng X Y, Li S J, Murr L E et al. J Mech Behav BiomedMater[J], 2012, 16: 153
[62] Ahmadi S, Yavari S, Wauthle R et al. Materials[J], 2015,8(4): 1871
[63] Li S J, Murr L E, Cheng X Y et al. Acta Materialia[J], 2012,60(3): 793
[64] Gibson L J, Ashby M F. Cellular Solids: Structure andProperties [M]. Cambridge: Cambridge University Press,1999
[65] Salda?a L, Vilaboa N. Acta Biomaterialia[J], 2010, 6(4):1649
[66] Akisue T, Thomas W B, Carol F F et al. Journal ofBiomedical Materials Research[J], 2001, 59(3): 507
[67] Lin T H, Yao Z Y, Sato T S et al. Acta Biomaterialia[J],2014, 10(8): 3747
[68] Li C D, Jiang C, Peng M Z et al. RSC Advances[J], 2018,8(4): 2229
[69] Markhoff J, Wieding J, Weissmann V et al. Materials[J],2015, 8(8): 5490
[70] Bael S Van, Chai Y C, Truscello S et al. Acta Biomater[J],2012, 8(7): 2824
[71] Taniguchi N, Fujibayashi S, Takemoto M et al. MaterialsScience and Engineering C[J], 2016, 59: 690
зӣёе…ій“ҫжҺҘ



















